
【题目】下列物质在水溶液中的电离方程式书写正确的是 ( )
A. Al2(SO4)3===2Al3++3SO![]() B. Cu(OH)2===Cu2++2OH-
B. Cu(OH)2===Cu2++2OH-
C. NaHSO4===Na++HSO![]() D. (NH4)2SO4===NH
D. (NH4)2SO4===NH![]() +SO
+SO![]()
科目:高中化学 来源: 题型:
【题目】在同温同压下,相同体积的甲、乙两种气体的质量比是17∶14。若乙气体是CO,则甲气体可能是( )
A. H2S B. HCl C. NH3 D. Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:

(1)固体I中主要成分为__________,捕获剂所捕获的气体主要是_________。
(2)处理含NH4+废水时,发生反应的离子方程式为___________。
(3)若X为适量空气,严格控制空气用量的原因是____________。
(4)工业废气中的SO2、NO还可采用NaClO2溶液作为吸收剂进行净化,在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323K,NaClO2溶液浓度为5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如下表:
离子 | SO42- | SO32- | NO3- | NO2- | Cl- |
c(mol·L-1) | 8.35×10-4 | 6.87×10-6 | 1.5×10-4 | 1.2×10-5 | 3.4×10-3 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式_________________。
增加压强,NO的转化率__________(填“提高”、“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐__________(填“增大”、“不变”或“减小”)。
③如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医院在进行外科手术时,常用HgCl2稀溶液作为手术刀的消毒剂,已知HgCl2有如下性质:①HgCl2晶体熔点较低 ②HgCl2熔融状态下不导电 ③HgCl2在水溶液中可发生微弱电离。下列关于HgCl2的叙述中正确的是( )
A. HgCl2晶体属于分子晶体
B. HgCl2属于离子化合物
C. HgCl2属于电解质,且属于强电解质
D. HgCl2属于非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式不正确的是( )
A. NaHCO3与NaOH溶液反应:HCO![]() +OH-===CO
+OH-===CO![]() +H2O
+H2O
B. 氢氧化铜溶液与硫酸反应:OH-+H+===H2O
C. 氯化铁溶液中加入足量的氨水:Fe3++3NH3·H2O===Fe(OH)3 ↓+3NH![]()
D. 盛放碱性试剂的溶液不能用玻璃塞的原因:SiO2+2OH-===SiO![]() +H2O
+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图Ⅰ、Ⅱ、Ⅲ是常见的气体发生装置;V、VI是气体收集装置,根据要求回求答下列问题:

(1)气体发生装置的选择:若用CaCO3与盐酸反应制CO2,则可选择_________(填序号);若用I装置制取氯气,则浓盐酸应盛放在__________(填I中的仪器名称)。写出实验室制取氯气的化学方程式_________________________________________。
(2)收集装置的选择:若选用V为氯气收集装置,则氯气应从__________口通入。
(3)实验室制取氯气,多余的氯气要进行尾气处理,一般将尾气通入到氢氧化钠溶液中,其发生反应的离子方程式为________________________________________。
(4)气体的吸收:若标准状况下1体积的水已吸收336体积的HCl,且得到的溶液的密度为1.08g/cm3,则所得溶液中溶质的物质的量浓度为________mol/L。(保留一位小数)

(5)实验室用右图装置(夹持及加热仪器已略)制备氯气并进行一系列相关实验。
①装置B中饱和食盐水的作用是___________;
②设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为___________色,打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是溶液分为两层,下层为 ___________色
③装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入________。
a | b | c | d | |
Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 无水氯化钙 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的。结合下列实验装置图回答问题:
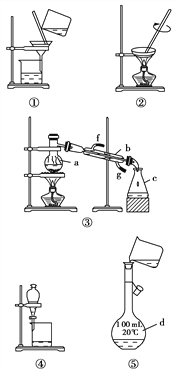
(1)写出上述五种实验操作的名称______________________________。
(2)写出图中字母所示的仪器的名称:a______,b___________, c________,d________。
(3)“粗盐提纯”实验中用到上述装置中的 ________(填序号)。
(4)若利用装置③分离乙酸(沸点118 ℃)和乙酸乙酯(沸点77.1 ℃)的混合物,还缺少的仪器有________,将仪器补充完整后进行的实验操作的名称为________;实验时仪器b中冷却水的进口为________(填“f”或“g”)。
(5)实验室现需要450 mL 0.1 mol/L的Na2CO3溶液,则需要用天平称量________g Na2CO3·10H2O固体;上图中的⑤是某同学转移溶液时的示意图,图中有两处错误分别是____________________________、
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com