
【题目】在电解水制取H2和O2时,为了增强导电性,常常要加入一些电解质,最好选用
A. H2SO4B. HC1
C. NaClD. NaOH
 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:
【题目】溴化钙是一种溴化物,用于石油钻井,也用于制造溴化铵及光敏纸、灭火剂、制冷剂等。制备CaBr2·2H2O的主要流程如下:

(1)与液溴的反应温度不能超过40℃的原因是 。
(2)滤渣的成分可能是 。
(3)试剂M是 ,加入M的目的是 。
(4)操作Ⅱ的步骤为蒸发浓缩、 、洗涤、干燥
(5)将氨气通入石灰乳,加入溴,于65°C进行反应也可制得溴化钙,此反应中还会生成一种无色气体,写出反应的化学方程式 。
(6)制得的CaBr2·2H2O可以通过以下方法测定纯度:称取5.00g样品溶于水,滴入足量Na2CO3溶液,充分反应后过滤,将滤渣洗涤、烘干、冷却,称量。得到2.00g固体,则CaBr2·2H2O的质量分数为 。(相对原子质量:Ca—40 Br—80 H—1 O—16)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水分子间存在一种叫“氢键”的作用(介于范德华力与化学键之间)彼此结合而形成(H2O)n。在冰中每个水分子被4个水分子包围形成变形的正四面体,通过“氢键”相互连接成庞大的分子晶体,其结构示意图如图所示。

(1)1 mol H2O形成的冰中有________mol“氢键”。
(2)水分子可电离生成两种含有相同电子数的微粒,其电离方程式为________。
(3)在冰晶体中除氢键外,还存在范德华力(11 kJ·mol-1)。已知冰的升华热是51 kJ·mol-1,则冰晶体中氢键的能量是________ kJ·mol-1。
(4)氨气极易溶于水的原因之一也是与氢键有关。请判断NH3溶于水后,形成的NH3·H2O的合理结构是________(填序号)。
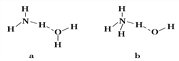
(5)NH3与PH3相比,热稳定性更强的是__________
(6)NH3、PH3在常温、常压下都是气体,但NH3比PH3易液化,其主要原因是____
A.键的极性N—H比P—H强
B.分子的极性NH3比PH3强
C.相对分子质量PH3比NH3大
D.NH3分子之间存在特殊的分子间作用力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质混合后,不能生成NaOH的是( )
A. Na和H2O B. Na2O2和H2O
C. Na2CO3和Ca(OH)2 D. NaCl和Ca(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2015·上海)离子方程式2Ca2+ + 3HCO3– + 3OH– → 2CaCO3↓ + CO32– + 3H2O可以表示( )
A.Ca(HCO3)2与NaOH溶液反应
B.NaHCO3与澄清石灰水反应
C.Ca(HCO3)2与澄清石灰水反应
D.NH4HCO3与澄清石灰水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,回答下列有关问题:

(1)在这些元素中,最活泼的金属元素和最活泼的非金属元素分别是____、______。(用元素符号作答)
(2)在这些元素的最高价氧化物对应水化物中,有一种呈两性的用来治疗胃酸过多反应的化学方程式______。
(3)在这些元素中,某元素的最高价氧化物对应的水化物可以和其气态氢化物反应,写出该化学方程式________。
(4)如何验证元素⑦与⑧的非金属性强弱,写出可以验证该结论的一个离子反应方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知在碱性溶液中可发生如下反应:2R(OH)3+3ClO-+4OH-=2RO4n-+3Cl-+5H2O。则RO4n-中R的化合价是( )
A.3
B.4
C.5
D.6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制取CuCl2的生产流程如下:

请结合下表数据,回答下列问题:
物 质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
⑴ 溶液A中加入NaClO的目的是 ;
此反应离子方程式为 ;
⑵ 在溶液B中加入CuO的作用是 ;
⑶ 操作a的目的是 ;
⑷ 在Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl2。采用多量盐酸和低温蒸干的目的是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com