
 ��
��
���� ��1��NaHCO3��Һ���Ҷ�����ҺӦ����C2O42-��������̼��ˮ��
��2���Ҷ���������KMnO4��Һ�ķ�Ӧ�У��̴�+7�۽�Ϊ+2�ۣ�̼��+3����Ϊ+4�ۣ����ݻ��ϼ���������ƽ��Ӧ�����ӷ���ʽ��
��3���Ҷ����������Ҵ���Ӧ�����Ҷ����������ע���ֹ������
��4�����Ҷ���ֽ⣬�����ɶ�����̼���壬��ʹ����ʯ��ˮ����ǣ�����CO2ʹ�����ֱ���壬����ʱ���������ݳ����������������Ʒ�Ӧ�����Ҷ���Ƴ�����Ҫ����֤�������ȷֽ⣬��Ҫ��ֹ�Ҷ���������ݳ����ݴ˴��⣮
��� �⣺��1��NaHCO3��Һ���Ҷ�����ҺӦ����C2O42-��������̼��ˮ����Ӧ����Ϊ����ɫ���ݲ�������Ӧ�����ӷ���ʽΪ HCO3-+H2C2O4=2H2O+2CO2��+C2O42-��
�ʴ�Ϊ������ɫ���ݲ����� HCO3-+H2C2O4=2H2O+2CO2��+C2O42-��
��2���Ҷ���������KMnO4��Һ�ķ�Ӧ�У��̴�+7�۽�Ϊ+2�ۣ�̼��+3����Ϊ+4�ۣ����ݻ��ϼ���������ƽ��Ӧ�����ӷ���ʽΪ2MnO4-+5H2C2O4+6H+=2Mn2++10CO2��+8H2O��
�ʴ�Ϊ��2��5��6��2��10��8��
��3B�е��ܿ���Һ���϶�������Һ���µ�ԭ���� ��ֹ���������ֹB��Һ�嵹����A�У����Ҷ����������Ҵ���ȫ�����Ļ�ѧ��Ӧ����ʽΪ ��
��
�ʴ�Ϊ����ֹ���������ֹB��Һ�嵹����A�У��� ��
��
��4��ͼ��٣��Թ������ʯ��ˮ�ȱ���ǣ����ֱ���壬��ԭ���Dz������ȷֽ����CO2��CO2ʹ����ʯ��ˮ����ǣ�����CO2ʹ�����ֱ���壬ͼ�����û������װ�ã��Ҷ���������ݳ��������Ҷ���Ƴ����������Թ������ʯ��ˮֻ����ǣ���������֤�������ȷֽ��װ���Ǣ٣���Ϊ������������������װ�ã�������������ݳ���
�ʴ�Ϊ���������ȷֽ����CO2��CO2ʹ����ʯ��ˮ����ǣ�����CO2ʹ�����ֱ���壻���ڴ������������ݳ�����ʯ��ˮ��Ӧ���ɲ���Ƴ������٣���������������װ�ã�������������ݳ���
���� ���⿼������ʵ���̽����������ѧ���ķ�����ʵ�������Ŀ��飬ע�����ʵ���ԭ����Ŀ�ĺͲ�����������Ŀ�Ѷ��еȣ�


 �ŵ������ϵ�д�
�ŵ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ɷǵ��������ˮ�õ�����Һ | |
| B�� | [H+]��[OH-]��Ϊ5.0��10-7mol•L-1����Һ | |
| C�� | �����ʵ�����ǿ����ǿ�Ӧ�õ�����Һ | |
| D�� | ��pH=9���ռ���Һϡ��100�����õ�����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
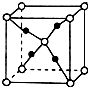 X��Y��Z��R��Ԫ�����ڱ���ǰ�������еij���Ԫ�أ�X�ĵ������ܶ���С�����壻Y��һ�ֺ��س����ڿ��ţ�����һ��ͬ���������ǽ���������֮һ��Z����̬�⻯����������������ˮ��������������������̣�R2+���ӵ�3d�����9�����ӣ�������ʱ�þ����Ԫ�ط��ţ�
X��Y��Z��R��Ԫ�����ڱ���ǰ�������еij���Ԫ�أ�X�ĵ������ܶ���С�����壻Y��һ�ֺ��س����ڿ��ţ�����һ��ͬ���������ǽ���������֮һ��Z����̬�⻯����������������ˮ��������������������̣�R2+���ӵ�3d�����9�����ӣ�������ʱ�þ����Ԫ�ط��ţ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������ˮֻ������ɢ���� | |
| B�� | ������������ˮֻ����ˮ������ | |
| C�� | ������������ˮ��ɢ����������������ˮ�Ϲ��̷ų������� | |
| D�� | ������������ˮ��ɢ������������С��ˮ�Ϲ��̷ų������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬ��ͬѹ�£�H2��g��+Cl2��g���T2HCl��g���ڹ��պ͵�ȼ�����µġ�H��ͬ | |
| B�� | �κ��������кͷ�Ӧ����1 mol H2O�Ĺ����У������仯����ͬ | |
| C�� | ��֪����2H2��g��+O2��g���T2H2O��g����H1��2H2��g��+O2��g��=2H2O��1����H2�����H1����2 | |
| D�� | ��֪����C��s��ʯī��+O2��g���TCO2��g����H=-393.5kJ•mol-1����C��s�����ʯ��+O2��g���TCO2��g����H=-395.0 kJ•mol-1 ��C��s��ʯī��=C��s�����ʯ����H=-1.5 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
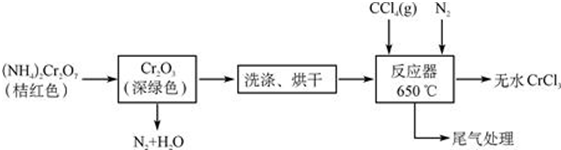
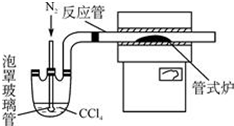
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ʊ�Fe��OH��3���壺��0.1mol•L-1FeCl3��Һ�м�������0.3mol•L-1NaOH��Һ | |
| B�� | ��ȥFeCl3��Һ������Cu2+����������Cu2+��FeCl3��Һ�м���������������ɫ�պ���ʧ����� | |
| C�� | ����1mol/LMgSO4��Һ����12.0gMgSO4���嵹��100mL����ƿ�У�Ȼ�����100mL����ˮ | |
| D�� | ȷ��Na2CO3��Һ���Ƿ����NaOH��ȡ������Һ�μӹ���BaCl2��Һ������ȡ��Һ������Һ�еμӷ�̪���۲��Ƿ���ֺ�ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
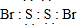 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 25��ʱ18 gˮ | |
| B�� | ��״���º�6.02��1023��ԭ�ӵ�Cl2 | |
| C�� | ��״����1 mol���� | |
| D�� | ���³�ѹ��44 g������̼ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com