
| A. | 溶液是无色透明的、均一的、稳定的混合物 | |
| B. | 浊液很不稳定,分散质颗粒在重力的作用下一定会向下沉淀 | |
| C. | 胶体在一定条件下能稳定住,属于稳定系 | |
| D. | 植物油溶入汽油中形成的分散系,为不稳定的乳浊液 |
分析 A.溶液可能有颜色;
B.密度小于水的难溶液体,与水形成乳状液时,分散质会向上漂浮;
C.胶体静置没有变化,属于稳定体系;
D.植物油易溶于汽油.
解答 解:A.溶液可能有颜色,如硫酸铜溶液为蓝色,液是透明的、均一的、稳定的混合物,故A错误;
B.密度小于水的难溶液体,与水形成乳状液时,静置分散质会向上漂浮,难溶于水的密度大于水的浊液,静置时分散质颗粒在重力的作用下一定会向下沉淀,故B错误;
C.胶体比较稳定,静置时不会分层或形成沉淀,所以胶体属于稳定体系,故C正确;
D.植物油易溶于汽油,植物油溶入汽油中形成的分散系属于稳定体系,不是乳状液,故D错误.
故选C.
点评 本题考查了分散系的性质,涉及胶体、溶液和浊液,侧重于基础知识的考查,题目难度不大.


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,关于该分子说法正确的是( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,关于该分子说法正确的是( )| A. | 含有碳碳双键、羟基、醛基、羧基 | |
| B. | 可以发生加成、加聚、取代、氧化等反应 | |
| C. | 含有2个手性碳原子 | |
| D. | S-诱抗素制剂的分子式为C15H20O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气态 | B. | 液态 | C. | 固态 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 酸性氧化物 | 一元酸 | 强电解质 | 分散系 | |
| A | Mn2O7 | 丙酸 | 三氧化二铝 | 黄河水 |
| B | NO2 | 高氯酸 | 盐酸 | 有色玻璃 |
| C | SiO2 | 石炭酸 | 氢氧化铝 | 云、雾 |
| D | SO2 | 硝酸 | 溴化氢 | 冰水混合物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
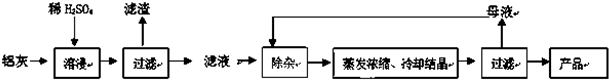
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.8 | 6.3 | 2.7 |
| 完全沉淀时 | 5.2 | 9.7 | 3.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 部分结构和性质 |
| A | 所有元素中原子半径最小 |
| B | 次外层电子数为最外层电子数的一半 |
| C | 单质由双原子分子构成,分子中有14个电子 |
| D | 地壳中含量最高的元素 |
| E | 最高价氧化物对应的水化物能溶于强酸和强碱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com