

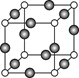
| A.砷化镓晶胞结构与NaCl相同 |
| B.GaP与GaAs互为等电子体 |
| C.电负性:As>Ga |
| D.砷化镓晶体中含有配位键 |
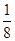 +6×
+6×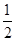 =4,而镓原子周围是4个均匀分布的砷原子为正四面体型。(3)NH3分子间有氢键沸点最高,其它分子按分子量大小排列,NH3>AsH3>PH3。(4)镓原子与3个甲基结合,且镓的价电子都成键,所以为sp2杂化。(5)砷的非金属性强,第一电离能大。(6)砷化镓晶胞与NaCl不同,A项错误。GaP与GaAs原子个数比相同,但电子总数不同,B项错误。As非金属性强,电负性也强,C正确。镓有3个价电子,但形成4个共价键,说明有一个配位键。D正确。
=4,而镓原子周围是4个均匀分布的砷原子为正四面体型。(3)NH3分子间有氢键沸点最高,其它分子按分子量大小排列,NH3>AsH3>PH3。(4)镓原子与3个甲基结合,且镓的价电子都成键,所以为sp2杂化。(5)砷的非金属性强,第一电离能大。(6)砷化镓晶胞与NaCl不同,A项错误。GaP与GaAs原子个数比相同,但电子总数不同,B项错误。As非金属性强,电负性也强,C正确。镓有3个价电子,但形成4个共价键,说明有一个配位键。D正确。

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源:不详 题型:填空题
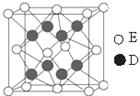
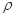 g·cm-3,阿伏加德罗常数为NA,
g·cm-3,阿伏加德罗常数为NA,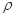 、NA的计算式表示)
、NA的计算式表示)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
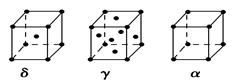
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | CH4 | SiH4 | NH3 | PH3 |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1 073 | 713.2 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 | 0.8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
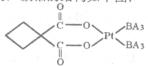
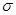 键
键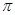 键
键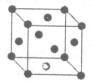
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
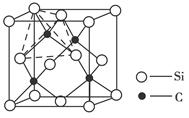
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
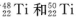 两种原子,它们互称为____。元素在元素周期表中的位置是第_____周期,第____族;基态原子的电子排布式为_____;按电子排布Ti元素在元素周期表分区中属于_____区元素。
两种原子,它们互称为____。元素在元素周期表中的位置是第_____周期,第____族;基态原子的电子排布式为_____;按电子排布Ti元素在元素周期表分区中属于_____区元素。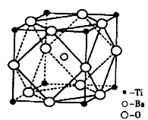
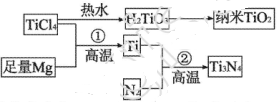 。
。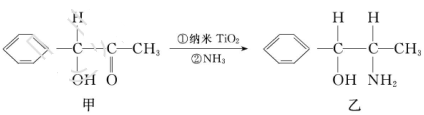
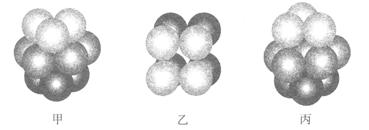
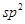 杂化的碳原子个数为_____,化合物乙中采取
杂化的碳原子个数为_____,化合物乙中采取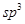 杂化的原子的第一电离能由大到小的顺序为_____。
杂化的原子的第一电离能由大到小的顺序为_____。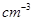 (NA为阿伏加德罗常数的数值,只列算式)。
(NA为阿伏加德罗常数的数值,只列算式)。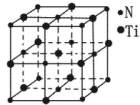
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com