
 nW(g)����H��ij��ѧ��ȤС���ͬѧ���ݴ˷�Ӧ�ڲ�ͬ�����µ�ʵ�����ݣ���������������ͼ��
nW(g)����H��ij��ѧ��ȤС���ͬѧ���ݴ˷�Ӧ�ڲ�ͬ�����µ�ʵ�����ݣ���������������ͼ��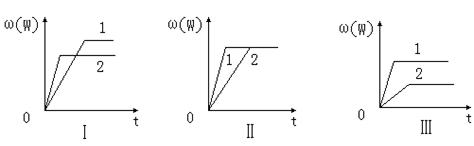
| A��ͼ������Dz�ͬѹǿ�Է�Ӧ��Ӱ�죬��p2��p1��a��b��n |
| B��ͼ������Dz�ͬѹǿ�Է�Ӧ��Ӱ�죬��p1��p2��n��a��b |
| C��ͼ���������ͬ��ͬѹ�´����Է�Ӧ��Ӱ�죬��1ʹ�õĴ���Ч���� |
| D��ͼ������Dz�ͬ�¶ȶԷ�Ӧ��Ӱ�죬��T1��T2����H��0 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
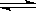 H2(g) + I2(g)���ﵽ ƽ��״̬�ı�־��
H2(g) + I2(g)���ﵽ ƽ��״̬�ı�־�� | A��I2(g)���������ʵ���H2���������� |
| B�������и���ֵ�Ũ�Ȳ���ʱ��仯 |
| C�������������ѹǿ���ٱ仯 |
| D����λʱ��������n mol H2��ͬʱ����n mol HI |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C��������H < 0��������淴Ӧ����ȷͼ��Ϊ�� ��
2C��������H < 0��������淴Ӧ����ȷͼ��Ϊ�� ��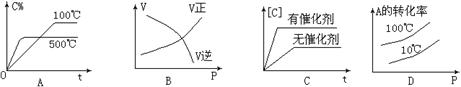
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
 2NH3(g)����H=-92.2kJ��mol-1��ƽ��ʱ����������ѹǿΪ��ʼʱ��80������д��������̣�
2NH3(g)����H=-92.2kJ��mol-1��ƽ��ʱ����������ѹǿΪ��ʼʱ��80������д��������̣� CH3OH(g)������5 min��ﵽƽ��״̬������ʱ���CH3OH������Ũ��Ϊ2 mol/L����д��������̣�
CH3OH(g)������5 min��ﵽƽ��״̬������ʱ���CH3OH������Ũ��Ϊ2 mol/L����д��������̣��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
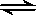 4NO2(g)+ O2(g)����Ӧ5min���N2O5�����ʵ���Ϊ2mol����(Ҫ��д��ϸ�������)
4NO2(g)+ O2(g)����Ӧ5min���N2O5�����ʵ���Ϊ2mol����(Ҫ��д��ϸ�������)�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g) ����ӦΪ���ȷ�Ӧ��ƽ���ƶ���ϵ���ߣ�����˵����ȷ����
2C(g) ����ӦΪ���ȷ�Ӧ��ƽ���ƶ���ϵ���ߣ�����˵����ȷ����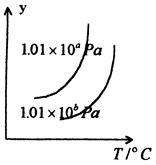
| A��a��b��y��ָB���������� |
| B��a��b��y��ָC���������� |
| C��a��b��y��ָA��ת���� |
| D��a��b��y��ָA��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Z(g)���˷�Ӧ�ﵽƽ��ı�־��
2Z(g)���˷�Ӧ�ﵽƽ��ı�־�� | A�������������ܶȲ���ʱ��仯 |
| B��v (X): v (Y)= l��2 |
| C��������X��Y��Z��Ũ�Ȳ���ʱ��仯 |
| D����λʱ������0.1 molXͬʱ����0.2molZ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NH3(g) ����H����92.4kJ/mol��
2NH3(g) ����H����92.4kJ/mol��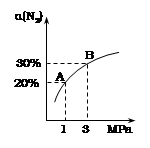
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com