
分析 题中涉及反应有RCOOR'+H2O→RCOOH+R'OH,NaOH+HCl=NaCl+H2O,n(NaOH)=0.03L×1mol/L=0.03mol,n(HCl)=0.04L×0.25mol/L=0.01mol,结合反应的方程式计算.
解答 解:(1)由RCOOR'+H2O→RCOOH+R'OH,NaOH+HCl=NaCl+H2O可知,n(酯)=0.03L×1mol/L-0.04L×0.25mol/L═O.O2mol,
M(酯)═$\frac{1.48g}{0.02mol}$=74g/mol,
则有机物分子式为:C3H6O2,
答:有机物分子式为C3H6O2;
(2)A为酯,分子式为C3H6O2,则可能结构为:HCOOCH2CH3,CH3COOCH3.
答:A可能的结构简式为HCOOCH2CH3,CH3COOCH3.
点评 本题考查机物的分子式的确定,为高频考点,侧重于学生的分析、计算能力的考查,注意把握酯化反应的特点,结合反应的方程式计算该题,难度中等.


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:解答题
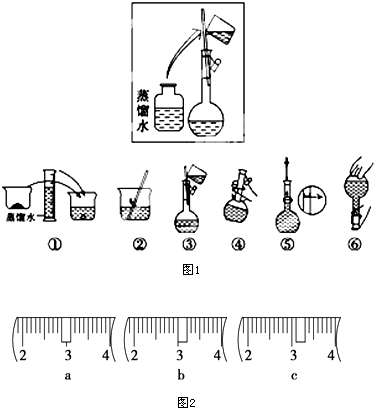 某同学帮助水质检测站配制230mL、1mol•L-1NaOH溶液以备使用.
某同学帮助水质检测站配制230mL、1mol•L-1NaOH溶液以备使用.| a | b | c | d | e | |
| 砝码大小/g | 100 | 50 | 20 | 10 | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色 | |
| B. | 发生硝化反应时,苯需要加热,甲苯在常温下就能进行 | |
| C. | 苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应 | |
| D. | 乙烯能发生加成反应,乙烷不能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| X(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| X(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
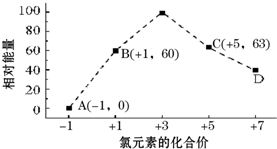 元素周期表中第ⅦA族元素的单质及其化合物的用途广泛.
元素周期表中第ⅦA族元素的单质及其化合物的用途广泛.
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
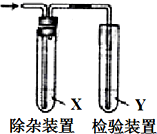 用如图所示装置检验气体时试剂X没必要或是错误的是( )
用如图所示装置检验气体时试剂X没必要或是错误的是( )| 检验的气体 | 试剂X | 试剂Y | |
| A | CH3CH2Br与NaOH乙醇溶液共热制备的乙烯 | H2O | Br2的CCl4溶液 |
| B | CH3CH2OH与浓H2SO4共热170℃制备的乙烯 | NaOH溶液 | 酸性KMnO4溶液 |
| C | 电石与饱和食盐水反应制备的乙烯 | 水 | 酸性KMnO4溶液 |
| D | 苯,液溴,铁屑混合反应生成的HBr | CCl4 | 硝酸银溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com