
【题目】2.3g某有机物A完全燃烧后,生成0.1molCO2和 2.7gH2O,测得该化合物的蒸气与空气的相对密度是1.6,已知此有机物可以与Na发生置换反应,写出此有机物与乙酸发生酯化反应的化学方程式 .
【答案】2C2H5OH+2Na=2C2H5ONa+H2↑
【解析】解:n(CO2)=0.1mol,则2.3g有机物中:n(C)=n(CO2)=0.1mol,m(C)=0.1mol×12g/mol=1.2g,
n(H2O)= ![]() =0.15mol,则2.3g有机物中:n(H)=2n(H2O)=0.3mol,m(H)=0.3mol×1g/mol=0.3g,因(1.2g+0.3g)<2.3g,所以有机物中还应还用O元素,且m(O)=2.3g﹣1.2g﹣0.3g=0.8g,n(O)=
=0.15mol,则2.3g有机物中:n(H)=2n(H2O)=0.3mol,m(H)=0.3mol×1g/mol=0.3g,因(1.2g+0.3g)<2.3g,所以有机物中还应还用O元素,且m(O)=2.3g﹣1.2g﹣0.3g=0.8g,n(O)= ![]() =0.05mol,该化合物的蒸气与空气的相对密度是1.6,则有机物A的相对分子质量=29×1.6=46,有机物A中:n(C):n(H):n(O)=0.1mol:0.3mol:0.05mol=2:6:1,所以该有机物的最简式为C2H6O,而C2H6O的相对分子质量为46,所以该有机物的分子式为C2H6O,此有机物可以与Na发生置换反应,说明含有羟基,应为乙醇,有机物与乙酸发生酯化反应的方程式为2C2H5OH+2Na=2C2H5ONa+H2↑,所以答案是:2C2H5OH+2Na=2C2H5ONa+H2↑.
=0.05mol,该化合物的蒸气与空气的相对密度是1.6,则有机物A的相对分子质量=29×1.6=46,有机物A中:n(C):n(H):n(O)=0.1mol:0.3mol:0.05mol=2:6:1,所以该有机物的最简式为C2H6O,而C2H6O的相对分子质量为46,所以该有机物的分子式为C2H6O,此有机物可以与Na发生置换反应,说明含有羟基,应为乙醇,有机物与乙酸发生酯化反应的方程式为2C2H5OH+2Na=2C2H5ONa+H2↑,所以答案是:2C2H5OH+2Na=2C2H5ONa+H2↑.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】下列有关晶体的说法中正确的是
A. 原子晶体中,共价键越强,熔点越高
B. 冰熔化时,水分子中共价键发生断裂
C. 氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子晶体
D. 碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子间的作用力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向碘水中加入适量CCl4并振荡,静置后观察到的现象是
A. 形成均匀的无色溶液
B. 形成均匀的紫红色溶液
C. 液体分层,下层呈紫红色
D. 液体分层,上下层均呈无色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可用如图所示装置制取少量乙酸乙酯(酒精灯等在图中均已略去).请填空: 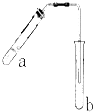
(1)试管a中需加入浓硫酸、冰醋酸和乙醇各2mL,正确的加入顺序用操作是 .
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是 .
(3)实验中加热试管a的目的是:; .
(4)试管b中加有饱和Na2CO3溶液,其作用是 .
(5)反应结束后,振荡试管b,静置.反应结束后,试管B内的液体分成两层,乙酸乙酯在层(填写“上”或“下”).若分离10mL该液体混合物需要用到的主要玻璃仪器是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A.乙醇和乙酸都存在碳氧双键B.甲烷和乙烯都可以与氯气反应
C.高锰酸钾可以氧化苯和甲烷D.乙烯可以与氢气发生加成反应,苯不能与氢气加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】储存浓硫酸的铁罐外口出现严重的腐蚀现象,这体现了浓硫酸的
A. 脱水性和吸水性 B. 吸水性和酸性
C. 强氧化性和吸水性 D. 不挥发性和酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,10 mL 0.40 mol/L H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)( )
A. 0~6 min的平均反应速率: v(H2O2)≈3.3×10-2mol·L-1·min-1
B. 0~6 min的平均反应速率: v(H2O2)<3.3×10-2mol·L-1·min-1
C. 反应至6 min时,c(H2O2)=0.30 mol/L
D. 反应至6 min时,H2O2分解了50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.2 mol·L-1的一元酸HA与等浓度NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )

A. HA为强酸
B. 该混合溶液pH=7.0
C. 该混合溶液中:c(A-)+c(Y)=c(Na+)
D. 图中X表示HA,Y表示OH-,Z表示H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com