
| A、升高温度可以增大化学反应速率 |
| B、将木炭粉碎成粉末可以加快反应速率 |
| C、增大压强可以增大化学反应速率 |
| D、增大炭的用量可以加快反应速率 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 已知化学反应N2+3H2=2NH3的能量变化如图所示,
已知化学反应N2+3H2=2NH3的能量变化如图所示,| 1 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5NA个H2所占的体积约为11.2L |
| B、1 mol OH-所含的电子数为9NA |
| C、标准状况下,9g H2O所占的体积约为11.2L |
| D、标准状况下,28 g CO和N2混合气体的体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Fe2+、SO42-、OH- |
| B、Na+、H+、Cl-、HCO3- |
| C、K+、Ag+、NO3-、Cl- |
| D、K+、Cu2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CuSO4溶液与Ba(OH)2溶液反应:Ba2++SO42-=BaSO4↓ |
| B、NaHSO4溶液和NaHCO3溶液反应:H++HCO3-=H2O+CO2↑ |
| C、氨水与醋酸混合:NH3?H2O+H+=NH4++H2O |
| D、H2SO4溶液与Mg (OH)2溶液反应:Mg2++2 OH-+2 H++SO42-=MgSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解时选用Fe作阳极,石墨棒作阴极 |
| B、阴极附近的沉淀只有Cr(OH)3 |
| C、阳极附近溶液中,发生反应的离子方程式是Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O |
| D、消耗1mol Cr2O72-,将有336g Fe消耗,因此要定期更换铁电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、催化性 | B、氧化性 |
| C、还原性 | D、既有氧化性又有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、氢气跟氧气反应生成水的同时释放能量 | ||
| B、氢气跟氧气反应生成水的同时吸收能量 | ||
C、1mol H2跟
| ||
| D、2mol H2(g)跟1mol O2(g)反应生成2mol H2O(g)释放能量490kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
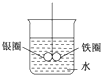 如图所示的装置,在铁圈和银圈的焊接处,用一根棉线将其悬吊在盛水的烧杯中,使之平衡.小心地向烧杯中央滴入CuSO4溶液,片刻后可观察到的现象是( )
如图所示的装置,在铁圈和银圈的焊接处,用一根棉线将其悬吊在盛水的烧杯中,使之平衡.小心地向烧杯中央滴入CuSO4溶液,片刻后可观察到的现象是( )| A、铁圈和银圈左右摇摆不定 |
| B、保持平衡状况 |
| C、银圈向下倾斜 |
| D、铁圈向下倾斜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com