
| A.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,则H2SO4和Ba(OH)2反应的反应热ΔH=2×(-57.3) kJ·mol-1 |
B.燃料电池中将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+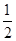 O2(g)===CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1,则CH3OH(g)的燃烧热为192.9 kJ·mol-1 O2(g)===CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1,则CH3OH(g)的燃烧热为192.9 kJ·mol-1 |
| C.H2(g)的燃烧热是285.8 kJ·mol-1,则2H2O(g)===2H2(g)+O2(g) ΔH=571.6 kJ·mol-1 |
D.葡萄糖的燃烧热是2 800 kJ·mol-1,则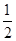 C6H12O6(s)+3O2(g)===3CO2(g)+3H2O(l) ΔH=-1 400 kJ·mol-1 C6H12O6(s)+3O2(g)===3CO2(g)+3H2O(l) ΔH=-1 400 kJ·mol-1 |
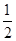 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l)△H=-1400kJ?mol-1,故D正确;故选D。
C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l)△H=-1400kJ?mol-1,故D正确;故选D。

科目:高中化学 来源:不详 题型:单选题
 CH3OH(g)
CH3OH(g)| | 10 min | 20 min | 30 min | 40 min | 50 min | 60 min |
| 300℃ | 0.080 | 0.120 | 0.150 | 0.168 | 0.180 | 0.180 |
| 500℃ | 0.120 | 0.150 | 0.156 | 0.160 | 0.160 | 0.160 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:推断题


 2HCl(g)+O2(g)△H>0.
2HCl(g)+O2(g)△H>0. O2(g)= H2O(1), △H2 = -285.84kJ·mol-l
O2(g)= H2O(1), △H2 = -285.84kJ·mol-l查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
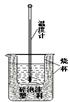
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Q1 + Q2 > Q3 | B.Q1 + Q2 > 2Q3 | C.Q1 + Q2 < Q3 | D.Q1+ Q2 < 2Q3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.①② | B.②③ | C.③④ | D.②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.生石灰和水的反应 |
| B.石灰石在高温下的分解反应 |
| C.盐酸与氢氧化钠溶液的反应 |
| D.木炭在氧气中燃烧 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
 。
。 | A.使用催化剂 | B.提高氧气的浓度 |
| C.提高反应的温度 | D.降低反应的温度 |

| 化学键 | H—H | O=O | H—O |
键能 | 436 | 496 | 463 |
 。其中,氢气在________(填“正”或“负”)极发生________反应(填“氧化”或“还原”)。电路中每转移0.2mol电子,标准状况下消耗H2的体积是________L。
。其中,氢气在________(填“正”或“负”)极发生________反应(填“氧化”或“还原”)。电路中每转移0.2mol电子,标准状况下消耗H2的体积是________L。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.凡需加热的反应一定是吸热反应 |
| B.只有分解反应才是吸热反应 |
| C.使用催化剂的反应是吸热反应 |
| D.酸碱中和反应的逆反应是吸热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com