
| A. | ①③④ | B. | ①②⑤⑥ | C. | ②⑤⑥ | D. | ①②④ |
分析 如果将Na2O、NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为同一类物质,就要分析这些物质的共同点,据此来分析.
解答 解:①Na2O、NaOH、Na2CO3、NaCl、Na2SO4都是由两种或两种以上元素构成的纯净物,属于化合物,故①正确;
②Na2O和NaOH与硝酸反应生成硝酸钠和水,Na2CO3和硝酸反应生成硝酸钠、二氧化碳和水,NaCl、Na2SO4与硝酸不反应,故②错误;
③Na2CO3、NaCl、Na2SO4是钠盐,都能溶于水,NaOH是可溶性强碱,Na2O能与水反应生成NaOH,Na2O因反应而溶于水,故③正确;
④Na2O属于金属氧化物、NaOH属于强碱、Na2CO3属于盐、NaCl属于盐、Na2SO4属于盐,它们在水溶液中能导电,属于电解质,故④正确;
⑤Na2O由钠元素和氧元素组成,属于氧化物;NaOH属于碱,NaCl、Na2SO4属于盐,G故⑤错误;
⑥NaCl由钠元素和氯元素组成,不属于钠的含氧化合物,故⑥错误.
分类标准正确的是①③④.
故选A.
点评 本题既考查了物质的分类,又考查了化合物的性质,找出它们的共同点是解题的关键,题目难度中等.


 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 一定温度下,甲酸加水稀释过程中溶液的导电能力如图所示曲线,请回答:
一定温度下,甲酸加水稀释过程中溶液的导电能力如图所示曲线,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 | |
| B. | 沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4]2+ | |
| C. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 | |
| D. | 向反应后的溶液加入乙醇,溶液没有发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
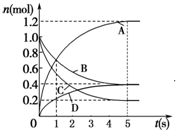 一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )| A. | 该反应的化学方程式为6A+2 D?3B+4C | |
| B. | 反应进行到1 s时,v(A)=v(B) | |
| C. | 反应进行到5 s时,B的平均反应速率为0.06mol/(L•s) | |
| D. | 反应进行到5 s时,v(A)=v(B)=v(C)=v(D) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 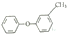 的同分异构体中,有醇、酚、酯类物质 的同分异构体中,有醇、酚、酯类物质 | |
| B. | 1mol 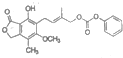 最多能与含5.0molNaOH的水溶液完全反应 最多能与含5.0molNaOH的水溶液完全反应 | |
| C. | 纯净物C4H8的氢种类最多为3种 | |
| D. | 化学式为C8H8的有机物,一定能和溴水发生加成反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com