
分析 设出一氧化氮、二氧化氮的体积,然后根据二氧化碳气体体积和溶液质量增加的量列方程组解出一氧化氮和二氧化氮的体积,从而得出其体积之比.
解答 解:设NO的物质的量是x,NO2的物质的量是y,
发生反应有:①NO+NO2+Na2CO3═2NaNO2+CO2、②2NO2+Na2CO3═NaNO3+NaNO2+CO2,
发生反应①NO为x,同时消耗二氧化氮的物质的量为x,则参加反应②的二氧化氮为y-x,则生成二氧化碳的物质的量为:x+$\frac{y-x}{2}$=$\frac{2.24}{22.4}$,
根据质量守恒定律可知,反应后溶液增加的质量为NO、NO2气体总质量-二氧化碳气体质量,即:30x+46y-$\frac{2.24}{22.4}$×44=3.6,
联立两个方程解得:x=$\frac{3}{40}$mol、y=$\frac{1}{8}$mol,
即:一氧化氮和二氧化氮的物质的量之比为:$\frac{3}{40}$mol:$\frac{1}{8}$mol=3:5,
所以相同条件下,一氧化氮和二氧化氮的体积之比是3:5,
故答案为:3:5.
点评 本题考查了混合物反应的计算,题目难度中等,明确质量守恒定律、差量法在化学计算中的应用,试题侧重考查学生的分析、理解能力能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、SO${\;}_{4}^{2-}$、NO${\;}_{3}^{-}$ | B. | K+、NO${\;}_{3}^{-}$、CO${\;}_{3}^{2-}$ | ||
| C. | Na+、K+、SO${\;}_{3}^{2-}$ | D. | Na+、NO${\;}_{3}^{-}$、SO${\;}_{3}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
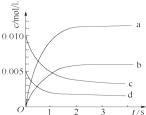 在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间变化如表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式相同的不同物质一定是同分异构体 | |
| B. | 通式相同的不同物质一定属于同系物 | |
| C. | 相对分子质量相同的不同物质一定是同分异构体 | |
| D. | 分子式相同,元素的质量分数也相同的物质是同种物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com