
根据元素周期律和物质结构的有关知识,以下有关排序错误的是( )
| A.离子半径:S2->Cl->Ca2+ | B.原子半径:Ca>S>Cl |
| C.酸性:HClO4<HBrO4<HIO4 | D.热稳定性:HCl>H2S>H2Se |
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍。下列说法正确的是( )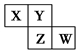
| A.元素W的最高价氧化物对应水化物的酸性最强 |
| B.单核阴离子半径的大小顺序为:r(W)>r(Z) >r(Y) |
| C.元素Y和元素Z的氢化物中均只存在极性共价键 |
| D.元素Y和元素Z的最高正化合价相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
A、B、C、D都是短周期元素,原子半径:D>C>A>B。已知A、B同周期,A、C同主族,C原子核内的质子数等于A、B原子核内的质子数之和,C原子最外层电子数是D原子最外层电子数的3倍。下列说法中正确的是
A.A、C两元素处在元素周期表中的第ⅥA族
B.B、D两元素组成的离子化合物中阴、阳离子的个数比为3∶1
C.B、C、D三种元素组成的化合物的化学式为DCB2
D.B、C、D三种元素的简单离子的半径大小顺序为:C>D>B
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于s轨道及s电子云,下列说法正确的是( )。
| A.某原子s轨道的能量随主量子数n的增大而增大 |
| B.s电子在以原子核为中心的球面上出现,但其运动轨迹测不准 |
| C.s能级有自旋方向相反的两原子轨道 |
| D.s轨道的电子云图为球形,说明电子在空间各位置出现的机会相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
自从1803年英国化学家、物理学家道尔顿提出了原子假说,人类对原子结构的认识就不断深入、发展,并通过实验事实不断地完善对原子结构的认识。下列关于原子结构模型的说法中,正确的是( )。
| A.道尔顿的原子结构模型将原子看作实心球,故不能解释任何问题 |
| B.汤姆逊“葡萄干布丁”原子结构模型成功地解释了原子中的正负粒子是可以稳定共存的 |
| C.卢瑟福核式原子结构模型指出了原子核和核外电子的质量关系、电性关系及占有体积的关系 |
| D.玻尔电子分层排布原子结构模型引入了量子化的概念,能够成功解释所有的原子光谱 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
四种主族元素的离子aXm+、bYn+、cZn-和dRm-(a、b、c、d为元素的原子序数),它们具有相同的电子层结构,若m>n,则下列叙述正确的是( )。
①a-b=n-m ②元素的原子序数:a>b>c>d ③元素非金属性:Z>R ④最高价氧化物对应的水化物的碱性:X>Y
| A.只有③ | B.①②③④ | C.①②③ | D.②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述错误的是( )。
| A.在所有元素中氢原子半径最小 |
| B.Al3+、Na+、O2-微粒半径依次增大 |
| C.P、S、Cl最高正价依次升高 |
| D.锂、钠、钾、铷、铯单质的熔点逐渐升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法错误的是( )
| A.Na与Al为同周期元素,钠原子最外层有1个电子,铝原子最外层有3个电子,所以钠的金属性比铝强 |
| B.Na与Mg为同周期元素,且Mg的核电荷数比Na的大,所以钠的金属性比镁强 |
| C.NaOH为强碱,而Al(OH)3具有两性,所以钠的金属性比铝强 |
| D.Zn+2Fe3+=Zn2++2Fe2+,所以Zn的金属性比Fe强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com