
【题目】以下判断,结论正确的是
选项 | 项目 | 结论 |
A | 三种有机化合物:丙烯、氯乙烯、苯 | 分子内所有原子均在同一平面 |
B | 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 | 属于同一反应类型 |
C | 乙烯和苯都能使溴水褪色 | 褪色的原理相同 |
D | C4H9Cl的同分异构体数目(不考虑立体异构) | 共有4种 |
A. A B. B C. C D. D
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】在36g碳不完全燃烧所得气体中,CO占1/3体积,CO2占2/3体积,且
C(s)+1/2(g)=CO(g) △H=-110.5kJ/mol
CO(g)+1/2O2(g)=CO2(g) △H=-283kJ/mol
与这些碳完全燃烧相比,损失的热量是
A. 172.5kJ B. 1149kJ C. 283kJ D. 517.5kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫的化合物在工业上有广泛的应用,因此研究硫的化合物制备有着重要的意义.某同学拟采用下图装置(实验前已除尽装置内的空气)来制取焦亚硫酸钠(Na2S2O5).已知装置图l—II中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2=Na2S2O5
(l)装置I是用亚硫酸钠固体和浓硫酸制备二氧化硫气体,该装置中反应的化学方程式为______________;如果想控制反应速度,图2中可选用的发生装置是_______(填写字母).

(2)装置Ⅱ中有Na2S2O5晶体析出,要获得已析出的晶体可采取的分离方法是________________
(3)装置III用于处理尾气,可选用的最佳试剂是______________(填序号).
a、饱和食盐水 b、NaOH溶液 c、浓硫酸 d、饱和NaHCO3溶液
(4)Na2S2O5与稀硫酸反应放出SO2,其离子方程式为___________________
(5)工业制备得到产品Na2S2O5中含有杂质碳酸钠,检验产品中含有碳酸钠杂质所需试剂是___________(填编号)(已知Na2S2O5溶于水即生成NaHSO3)
①酸性高锰酸钾 ②品红溶液 ③澄清石灰水
④饱和碳酸氢钠溶液 ⑤NaOH ⑥稀硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一瓶溶液中可能含有Mg2+、Na+、OH-、Cl-、CO32-和SO42-中某几种,现分别取该溶液少量装于两支试管,进行以下实验:
①向第一支试管中滳入酚酞溶液,溶液变红;
②向第二支试管中加入足量BaCl2溶液,生成白色沉淀,过滤,并将滤液移入第三支试管,在沉淀中加入稀硝酸,沉淀逐渐消失并有无色无味气体产生,该气体通入澄清石灰水,石灰水变浑浊。
③向第三支试管中先加入硝酸酸化,再加入硝酸银溶液,出现白色沉淀,通过以上实验可判断溶液中含有离子为 ,不含有的离子为 ,无法确定是否含有的离子为 ,写出实验②③中所有有关反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中:
A.![]()
B.![]()
C.![]()
D.![]()
(1)水只作氧化剂的是 (填序号,下同),水只作还原剂的是 ,水既作氧化剂又作还原剂的是 。
(2)用双线桥表示D反应中电子转移情况。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336mL(标准状态)气体。请回答下列问题。
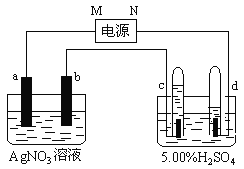
(1)直流电源中,N为 极。
(2)AgNO3溶液的浓度___________(填增大、减小或不变。下同),H2SO4溶液的pH ,若要硫酸恢复成原溶液需加入
(3)Pt电极上生成的物质是 ,其质量为 g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】DNA是控制遗传性状的遗传物质,在水稻的细胞中它分布在( )
A. 细胞核、内质网 B. 细胞核、核糖体
C. 细胞核、细胞质基质 D. 细胞核、线粒体、叶绿体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用右图装置完成下表所列的四个实验,不能达到实验目的是
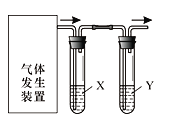
选项 | 实验目的 | 试剂X | 试剂Y |
A | 验证C2H5OH与浓H2SO4加热至170℃制得的乙烯的性质 | NaOH溶液 | Br2水 |
B | 检验FeSO4受热分解产生的气体中有SO3和SO2 | BaCl2溶液 | 品红溶液 |
C | 验证电石与饱和食盐水反应生成的乙炔的性质 | CuSO4溶液 | KMnO4溶液 |
D | 验证氧化性:Cl2>Br2>I2 | NaBr溶液 | KI溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷的常见酸性氧化物有As2O3和As2O5,根据图中信息回答下列问题:
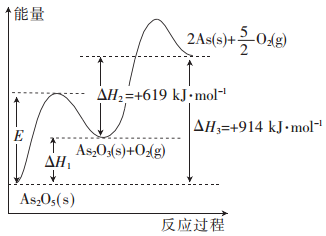
(1)As2O5分解生成As2O3和O2的反应中,加入催化剂,E__________(填“增大”、“减小”或 “不变”,下同),△H1_________。
(2)As2O3分解生成As和O2的热化学方程式为____________________。
(3)As2O3和O2反应生成As2O5的热化学方程式为_____________________。
(4)若1 mol As2O5分解生成0.4 mol As2O3和1.2 mol As,则该分解过程中,需吸收的总能量为_________kJ。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com