
下列有关化学用语使用不正确的是( )
|
| A. | 原子核内有18个中子的氯原子: |
|
| B. | S2﹣的结构示意图: |
|
| C. | 钒原子电子排布式:[Ar]3d34s2 |
|
| D. | NH4Br的电子式: |
考点:
常见元素的名称、符号、离子符号;电子式;原子结构示意图;原子核外电子排布.
专题:
化学用语专题.
分析:
A、依据质量数=中子数+质子数计算,依据原子符号的正确书写方法写出;
B、硫原子有哦16个核外电子,得到2个电子形成带两个负电荷的阴离子,依据离子结构写出离子结构示意图;
C、依据钒的电子亚层结构、能级变化、电子排布规律分析判断;
D、溴化铵是离子化合物,由溴离子和铵根离子构成,结合电子式书写方法写出判断.
解答:
解:A、依据质量数=中子数+质子数计算,A=17+18=35,依据原子符号的正确书写方法写出的原子符号为3517Cl,故A正确;
B、硫原子核外有16个核外电子,得到2个电子形成带两个负电荷的阴离子,离子结构示意图为, ,故B正确;
,故B正确;
C、依据钒的电子亚层结构、能级变化、电子排布规律分析写出,钒是第四周期,第五副族,电子亚层存在能级交错,原子电子排布式为:[Ar]3d34s2 ,故C正确;
D、溴化铵是离子化合物,由溴离子和铵根离子构成,结合电子式书写方法写出的电子式为,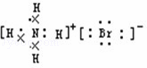 ,故D错误;
,故D错误;
故选D.
点评:
本题考查了化学用语的规范应用和书写原则,主要是原子符号、离子结构示意图,电子排布式,电子式的书写分析判断,题目较简单.


科目:高中化学 来源: 题型:
下列热化学方程式中,△H能正确表示物质的燃烧热的是( )
|
| A. | CO(g)+ |
|
| B. | C(s)+ |
|
| C. | H2(g)+ |
|
| D. | 2C8H18(l)+25O2(g)═16CO2(g)+18H2O(l);△H=﹣11036 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
稀氨水中存在下述电离平衡:NH3+H2O⇌NH3•H2O⇌NH4++OH﹣加入下列物质:请在答题卡上相应空格处填上:正向移动、逆向移动或不移动.
| 加入的物质 | NH4Cl | NH3 | NaOH |
| 平衡移动的方向 | (1) | (2) | (3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
一真空定容的密闭容器中盛有1mol PCl5,发生反应PCl5(g)⇌PCl3(g)+Cl2(g),一定条件下平衡时PCl5所占的体积百分数为M,若相同条件相同容器中,最初放入2mol PCl5,则平衡时,PCl5的体积百分数为N,下列结论正确的是( )
|
| A. | M>N | B. | M=N | C. | M<N | D. | 无法比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在100℃时,PH=7呈 性.
(2)碳酸钠溶液呈碱性的原因,用离子方程式表示: .
(3)氯化铝溶液呈酸性的原因,用离子方程式表示:
(4)写电离方程式NaHCO3
(5)由氢气和氧气反应生成1mol水蒸气放热241.8KJ,写出该反应的热化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
已知醋酸溶液中有如下平衡:CH3COOH⇌CH3COO﹣+H+,下列试剂能使CH3COOH的电离程度增大且c(H+)减小的是( )
|
| A. | CH3COOH | B. | H2O | C. | CH3COONa | D. | HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D四块金属片,进行如下实验:
①A、B用导线相连后,同时浸入稀硫酸溶液中,A极为负极;
②C、D用导线相连后,同时浸入稀硫酸溶液中,电流由D→导线→C;
③A、C相连后,同时浸入稀硫酸溶液中,C极产生大量气泡;
④B、D相连后,同时浸入稀硫酸溶液中,D极发生氧化反应.
据此,判断四种金属的活动性顺序是( )
|
| A. | A>B>C>D | B. | A>C>D>B | C. | C>A>B>D | D. | B>D>C>A |
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是
A.14g聚丙烯中含C-H键总数目为2NA
B.1molFe与足量的稀硝酸反应转移电子总数目为2NA
C.标准状况下,44.8L乙醛中含乙醛分子总数目为2NA
D.常温常压下,200g质量分数为17%H2O2溶液中含氧原子总数目为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com