
| 实验 | 试剂1 | 试剂2 | 操作及现象 |
| ① | 铜丝 | 氯气 | 将加热后的铜丝伸入盛有氯气的集气瓶中,产生棕黄色的烟 |
| ② | 稀硝酸 | 产生无色气体,遇空气变为红棕色 | |
| ③ | 0.1mol/LKMnO4溶液 | 加热后,铜丝表面有黑色物质,溶液颜色无明显变化 |
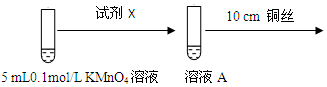
| 环境 | 反应现象 |
| 酸性 | 溶液紫红色变浅 |
| 碱性(1mL 1mol/L NaOH溶液) | 无明显现象 |
分析 Ⅰ.探究Cu的化学性质:(1)氧化还原反应中,失去电子的反应物为还原剂,表现还原性,铜为金属,在氧化还原反应中易失去电子,化合价升高,表现出还原性;
(2)铜和稀硝酸反应生成硝酸铜、一氧化氮和水;
(3)黄色与蓝色混合呈现绿色,氯化铜在溶液中为蓝绿色,氯化铜在溶液中以[Cu(H2O)4]2+存在,加水过程中,随着[Cu(H2O)4]2+的增加,其浓度不同,颜色不同;
【查阅资料】(4)铜在空气中加热生成氧化铜,在中性溶液中氧化铜不溶解,阻碍铜与KMnO4溶液反应.
Ⅱ.(1)因高锰酸钾具有强氧化性,所以选择酸为非还原性的酸;对照实验需除酸碱性不同,其它条件都相同,该实验需体积、浓度相同;
(2)①电化学腐蚀,正极上高锰酸根离子得电子生成锰酸根离子,锰酸根离子得电子生成棕褐色MnO2和氢氧根离子;
②将铜丝紧密缠绕在碳棒上放入碱性的溶液A中,试管底部出现棕褐色粉末,发生电化学腐蚀,说明碱性条件下铜单质可以与KMnO4溶液发生氧化还原反应,对照实验说明反应速度很慢,(或假设Ⅱ成立).
解答 解:Ⅰ.探究Cu的化学性质:(1)铜和氯气反应生成氯化铜,铜元素的化合价变化为0价升高为+2价,表现出还原性,铜与稀硝酸反应生成硝酸铜,铜元素的化合价变化为0价升高为+2价,表现出还原性,铜丝加热后,铜丝表面有黑色物质,生成氧化铜,铜元素的化合价变化为0价升高为+2价,表现出还原性,所以根据化合价分析,在化学反应中铜主要体现出的化学性质是还原性,
故答案为:还原性;
(2)铜和稀硝酸反应生成硝酸铜、一氧化氮和水,反应的离子方程式为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;
(3)氯化铜在溶液中:[CuCl4]2-+4H2O?[Cu(H2O)4]2++4 Cl-,以[Cu(H2O)4]2+存在,其浓度不同,颜色不同,加水过程中,平衡正向移动,随着[Cu(H2O)4]2+的增加,溶液由黄色变为绿色,最后变为蓝色,
故答案为:[CuCl4]2-+4H2O?[Cu(H2O)4]2++4 Cl-,加水过程中,平衡正向移动,随着[Cu(H2O)4]2+的增加,溶液由黄色变为绿色,最后变为蓝色;
【查阅资料】(4)铜在空气中加热生成氧化铜,反应③中溶液颜色无明显变化,是因为中性环境下,铜表面黑色的CuO,不溶解,阻碍铜与KMnO4溶液反应,
故答案为:生成的CuO覆盖在铜的表面阻止反应继续继续;
Ⅱ.(1)因高锰酸钾具有强氧化性,所以选择酸为非还原性的酸,所以探究酸性条件下反应时,试剂X是H2SO4溶液,对照实验需除酸碱性不同,其它条件都相同,如果加入H2SO4溶液的体积是1 mL,对比碱性条件下的实验现象,则能说明发生了反应,如果加入H2SO4溶液的体积是大于1 mL,则有可能是稀释作用导致的溶液颜色变浅,
故答案为:H2SO4溶液;如果加入H2SO4溶液的体积是1 mL,对比碱性条件下的实验现象,则能说明发生了反应,如果加入H2SO4溶液的体积是大于1 mL,则有可能是稀释作用导致的溶液颜色变浅;
(2)①电化学腐蚀,正极上发生还原反应,高锰酸根离子得电子生成锰酸根离子,MnO4-+e-→MnO42-,锰酸根离子得电子生成棕褐色MnO2和氢氧根离子,MnO42-+2e-+2H2O=MnO2+4OH-,
故答案为:MnO4-+e-→MnO42-、MnO42-+2e-+2H2O=MnO2+4OH-;
②探究溶液环境对反应的影响,将铜丝紧密缠绕在碳棒上放入碱性的溶液A中,溶液很快由紫红色变为深绿色,一段时间后,试管底部出现棕褐色粉末,发生电化学腐蚀,对照碱性(1mL 1mol/L NaOH溶液),无明显现象,说明碱性条件下铜单质可以与KMnO4溶液发生氧化还原反应,但反应速度很慢,(或假设Ⅱ成立),
答:碱性条件下铜单质可以与KMnO4溶液发生氧化还原反应,但反应速度很慢,(或假设Ⅱ成立).
点评 本题考查了探究Cu的化学性质及溶液环境对反应的影响实验,掌握铜及其化合物的性质以及高锰酸根的性质是解答关键,侧重学生实验能力和分析能力的考查,注意电化学高频考点的掌握,题目难度中等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
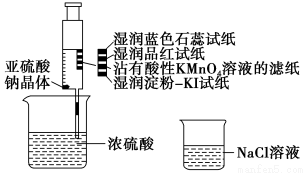
| A. | 蓝色石蕊试纸先变红后褪色 | |
| B. | 品红试纸、蘸有酸性KMnO4溶液的滤纸均褪色,证明SO2具有漂白性 | |
| C. | 湿润淀粉-KI试纸未变蓝说明SO2的氧化性弱于I2 | |
| D. | NaCl溶液可用于除去实验中多余的SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 250 | 350 |
| K | 2.041 | x |
| c(CO)/mol•L-1 | c(H2)/mol•L-1 | c(CH3OH)/mol•L-1 | |
| 0min | 0.8mol•L-1 | 1.6mol•L-1 | 0 |
| 2min | 0.6mol•L-1 | y | 0.2mol•L-1 |
| 4min | 0.3mol•L-1 | 0.6mol•L-1 | 0.5mol•L-1 |
| 6min | 0.3mol•L-1 | 0.6mol•L-1 | 0.5mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
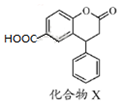
| A. | X的分子式为C16H11O4 | |
| B. | X分子中有三种不同的官能团 | |
| C. | 1 mol化合物X最多能与3 mol NaOH反应 | |
| D. | X分子中两个苯环一定处于同一平面 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com