
NH3��Ϊһ����Ҫ����ԭ�ϣ�������Ӧ���ڹ�ҵ�����������й����ʷ�Ӧ�Ĵ����о������������863�ƻ���
(1)���������н�ǿ��ѡ���ԣ���רһ�ԡ���֪��
��ӦI��4NH3(g) +5O2(g)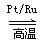 4NO(g) +6H2O(g) ��H= -905.0 kJ��mol-1
4NO(g) +6H2O(g) ��H= -905.0 kJ��mol-1
��ӦII:4NH3(g)+3O2(g) 2N2(g) +6H2O(g) ��H= -1266.6 kJ��mol-1
2N2(g) +6H2O(g) ��H= -1266.6 kJ��mol-1
д��NO�ֽ�����N2��O2���Ȼ�ѧ����ʽ_____��
(2)�ں��º���װ���г���һ������NH3��O2,��ij�����������½��з�ӦI ,��ò�ͬʱ���NH3��O2,��Ũ�����±���
ʱ��(min) | 0 | 5 | 10 | 15 | 20 | 25 |
c(NH3)/mol��L-1 | 1.00 | 0.36 | 0.12 | 0.08 | 0.072 | 0.072 |
c(O2)/mol• L-1 | 2.00 | 1.20 | 0.90 | 0.85 | 0.84 | 0.84 |
�������й���������ȷ����_____________��
A.ʹ�ô���ʱ���ɽ��÷�Ӧ�Ļ�ܣ��ӿ��䷴Ӧ����
B.�����������4v��(NH3) =6v��(H2O)ʱ��˵����Ӧ�Ѵ�ƽ��
C.��������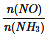 =1ʱ��˵����Ӧ�Ѵ�ƽ��
=1ʱ��˵����Ӧ�Ѵ�ƽ��
D.ǰ10�����ڵ�ƽ������v( NO)=0.088 mol��L-1��min-1
(3)��������ʱ�ᷢ����������������ӦI��II��Ϊ����ij�����Ը÷�Ӧ��ѡ���ԣ���1L�ܱ������г���1 mol NH3��2mol O2������й����ʵ�����ϵ����ͼ��
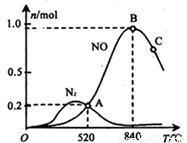
�ٸô����ڵ���ʱѡ��Ӧ_______(� I ���� II������
��52��ʱ��4NH3+3O2 2N2+6H2O��ƽ�ⳣ��K=_______(��Ҫ��ó���������ֻ���г����ּ���ʽ����
2N2+6H2O��ƽ�ⳣ��K=_______(��Ҫ��ó���������ֻ���г����ּ���ʽ����
��C���B����������NO�����ʵ����ٵ���Ҫԭ��________��
(4)�Ʊ�����ʱ������һ���ķ�Һ����ҵ�ϳ�������������ͳ�ȥ��Һ�е�Cu2+��
��֪��25��ʱ��K1(H2S) =1.3��10-7��K1(H2S) =7.1��10-15��Ksp(CuS) =8.5��10-45
���ڼ�����Һ�е�����Ũ��ʱ���漰����ĵ���ͨ��Ҫ���н��ƴ�������0.lmol •L-1�������pH��______(ȡ������������
��ijͬѧͨ�����Ƽ��㷢��0.lmol •L-1��������0.0lmol •L-1�������е�c(S2-)��ȣ����ҵ���_____mol��L-1
����֪��ij��Һ�ӽ������ԣ������������������ᣬ����Һ��c(Cu2+) >_____ mol��L-1(������������λ��Ч���֣����ͻ����CuS������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�����ʡ���������е�ʮ��У�ص���ѧ������һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ���������ͬһԭ�����͵���
A. Ʒ����Һ�зֱ�ͨ��SO2��Cl2��Ʒ�����ɫ
B. ��ˮ�ֱ����ֲ���ͺ��ѻ������У���ˮ����ɫ
C. ��������Һ�зֱ����NaCl��Һ��HgCl2��Һ�����й�������
D. �ֱ����ʢ��NH4Cl�͵��ʵ���Թܣ��ܿھ��й�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���Ĵ�ʡ��ɽ�и����ڶ��ε����о����������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ���������ֵ������˵����ȷ����
A. 0.2mol������������ϡ���ᷴӦ����������ķ���ЧĿΪ0.3NA
B. ���³�ѹ�£�14g��C2H4��C3H6��ɵĻ�������к���̼ԭ�ӵ���ĿΪNA
C. 2.24LCO2��������Na2O2��Ӧ��ת�Ƶĵ���������Ϊ0.1NA
D. 1L1mol/L��KAl(SO4)2��Һ������������Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���Ĵ�ʡ������ѧ�ڵ��Ĵ��¿������ۺϻ�ѧ�Ծ��������棩 ���ͣ������
�������ƿ������ڸ��Ƶر�ˮ�ʡ��������ؽ������ӷ�ˮ�������ೱ��Ҳ������Ӧ�������ȡ�ʵ���ҿ��ù�ҵ̼���(��MgCO3��FeCO3������)��ȡ������̼��ƣ�Ȼ�����ô���̼�����ȡ�������ƣ�����Ҫ�������£�
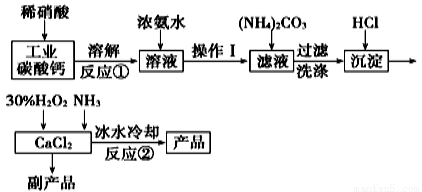
��֪��CaO2��8H2O�ʰ�ɫ����ˮ��
(1)д����Ӧ����������ԭ��Ӧ�����ӷ���ʽ�� ______________��
(2)��Ӧ�ٺ����Һ�м�Ũ��ˮ��Ŀ���ǣ� __________________��
(3)��Ӧ�ڳ��ñ�ˮ�����¶���0�����ң������ԭ����(д������)��
��__________________����______________��
(4)�ⶨ��Ʒ��CaO2�ĺ�����ʵ�鲽����
��һ����ȷ��ȡa g��Ʒ��������ƿ�У�������������ˮ������b g KI���壬�ٵ�������2 mol/L��H2SO4��Һ����ַ�Ӧ��
�ڶ�������������ƿ�м��뼸�ε�����Һ��
����������ε���Ũ��Ϊc mol��L��1��Na2S2O3����Һ����Ӧ�յ㣬����Na2S2O3��ҺV mL��
��֪��I2��2S2O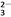 ===2I����S4O
===2I����S4O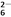 ��
��
�ٵζ��յ������Ϊ____________����Ʒ��CaO2����������Ϊ_________________
��ijͬѧ��һ���͵ڶ����IJ������ܹ淶������������̫����������õ�CaO2��������������________ (�����Ӱ�족��ƫ�͡���ƫ�ߡ�)��ԭ����_____________.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���Ĵ�ʡ������ѧ�ڵ��Ĵ��¿������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
������Ԫ��X��Y��Z��W��ԭ����������������ԭ������������֮��Ϊ16��Y��ԭ�Ӱ뾶��X �Ĵ�X��Wͬ���壬Z�ǵؿ��к�����ߵĽ���Ԫ�ء�����˵����ȷ����
A. ԭ�Ӱ뾶�Ĵ�С˳��: r(W)��r(Z)��r(Y)
B. Ԫ��X��Yֻ���γ�һ�ֻ�����
C. Ԫ��W�ļ���̬�⻯������ȶ��Ա�X��ǿ
D. Y��W�������������Ӧ��ˮ��������ܽ�Z����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ�Ƹ��и���3��������������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�±�ΪԪ�����ڱ��ж����ڵ�һ���֣�����YԪ�ص�ԭ������ΪM��NԪ��ԭ������֮�͡�����˵����ȷ����
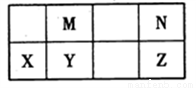
A. �⻯����ȶ��ԣ�N >Z������Ϊ���⻯����ӿ��γ����
B. Ԫ�صķǽ����ԣ�M > Y������Ϊ����M����YN2��Ӧ���ɵ���Y
C. �۷е㣺YN2>MN2������ΪYN2�ķ��Ӽ�������ǿ
D. �����ӵİ뾶��N >X������Ϊ���Ǿ�����ͬ�ĵ��Ӳ�ṹ��X�ĺ˵��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ��ɳ�г���������ظ���3��ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
�ԷϾ�Ǧ�����еĺ�Ǧ���ϣ�Pb��PbO��PbO2��PbSO4��̿�ڵȣ�Ϊԭ�ϣ��Ʊ���Ǧ��ʵ��Ǧ���������á��乤����������ͼ��ʾ��
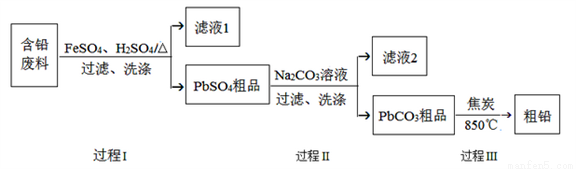
��֪��Ksp(PbSO4)=1.6��10-5,Ksp(PbCO3)=3.3��10-14.
��1�����̢��У���Fe2+���£�Pb��PbO2��Ӧ����PbSO4�Ļ�ѧ����ʽ��__________��
��2�����̢��У�Fe2+�����̿ɱ�ʾΪ��
i��2Fe2++ PbO2+4H++SO42- 2Fe3++PbSO4+2H2O
2Fe3++PbSO4+2H2O
ii: ����
��д��ii�����ӷ���ʽ��________________��
������ʵ�鷽����֤ʵ���������̡���ʵ�鷽������������
a.���ữ��FeSO4��Һ�м���KSCN��Һ����Һ������ɫ���ټ�������PbO2����Һ��졣
b.___________��
��3�����̢��Ŀ������������Һ2��c(SO42-)=1.6mol/L,c(CO32-)=0.1mol/L,��PbCO3��____����ǡ�������PbSO4��
��4�������ӽ���Ĥ�����ⷨ�ǴӺ�Ǧ��������ȡǦ��һ���¹��գ���װ����ͼ��ʾ������Ǧ����Ͷ�������ң���Ǧ�����е�PbSO4��NaOH��Һ�� ����Ӧ:PbSO4 + 3OH- = HPbO2-+ SO42- +H2O��
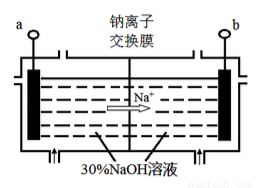
��a����ӵ�Դ��________��������
�ڵ������У�PbO2��PbO��HPbO2-�������ŵ磬����PbO2�ŵ�ĵ缫��ӦʽΪ___________��
���봫ͳ��Ĥ�����ⷨ��ȣ�ʹ�������ӽ���Ĥ���� ���PbԪ�ص������ʣ�ԭ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�갲��ʡ��һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��MgCl2��KCl��K2SO4�����εĻ����Һ�У���K����Cl����Ϊ1.5mol��Mg2��Ϊ0.5mol����SO42-�����ʵ���Ϊ ( )
A. 0.1mol B. 0.5mol C. 0.15mol D. 0.25mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ�ϲ��и�����һ��ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
�о�̼�������仯�����ת�����ڻ����ĸ������ش����塣
��1��������ԭ������NOx��ת�����£�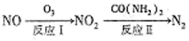
��֪��NO(g)+O3(g)=NO2(g)+O2(g) ��H=-200.9kJ/mol
2NO(g)��O2(g)=2NO(g) ��H=-116.2kJ/mol
��ӦI���Ȼ�ѧ����ʽΪ________________��
��2���������뽫CO�����з�Ӧ��ȥ��2CO(g)=2C(s)+O2(g) ��H>0����������������ܷ�ʵ�֣�______����ǡ���) ��������_____________��
��3��һ�������£�CO�����ĩ״�����������������ɼ����ơ���֪����ʱ������ĵ���ƽ�ⳣ��Ka=1.70��10-4��
�� �����Ƶ�ˮ��Һ�ʼ��ԣ��������ӷ�Ӧ����ʽ��ʾ��ԭ��___________��
�� ��20mL 0.1mol/L�ļ�������Һ�еμ�10ml 0.1mol/L�����ᣬ���Һ��______�ԣ���ᡱ�������Һ������Ũ�ȴӴ�С��˳��Ϊ______________��
��4������̿Ҳ�����ڴ�������β���е�NO����2L�����ܱ������м���0.1000molNO��2.030mol�������̿������A��B�������壬�ڲ�ͬ�¶��²��ƽ����ϵ�и����ʵ����ʵ������±���
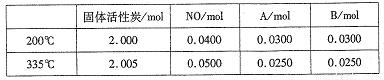
�ٸ÷�Ӧ������ӦΪ________(����ȡ����ȡ�)��Ӧ��
�� 200��ʱ��ƽ���������������ٳ���0.1molNO���ٴ�ƽ���NO�İٷֺ�����_____�������������С�����䡱����
�ۼ��㷴Ӧ��ϵ��335�� ʱ��ƽ�ⳣ��_______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com