
已知反应:2NO(g)+Br2(g) 2NOBr(g) △H=-a kJ·mol-1 (a>0),其反应机理如下
2NOBr(g) △H=-a kJ·mol-1 (a>0),其反应机理如下
①NO(g)+Br2(g) NOBr2(g) 快 ②NO(g)+NOBr2(g)
NOBr2(g) 快 ②NO(g)+NOBr2(g) 2NOBr(g) 慢
2NOBr(g) 慢
下列有关该反应的说法正确的是( )
A.该反应的速率主要取决于①的快慢
B.NOBr2是该反应的催化剂
C.正反应的活化能比逆反应的活化能小a kJ·mol-1
D.增大Br2(g)浓度能增大活化分子百分数, 加快反应速率
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源:2016-2017学年新疆兵团二师华山中学高一期中化学卷(解析版) 题型:选择题
下列状态的物质,既能导电又属于电解质的是
A.MgCl2晶体 B.NaCl溶液 C.液态氯化氢 D.熔融的KOH
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏拉萨中学高二上学期月考二化学卷(解析版) 题型:选择题
下列关于溶液酸碱性的说法正确的是( )
A.pH=7的溶液呈中性 B.中性溶液中一定有c(H+)=10-7mol/L
C.c(H+)=c(OH-)的溶液呈中性 D.在100℃时,纯水的pH<7,因此呈酸性
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:选择题
已知反应:C(s)+H2O(g) CO(g)+H2 (g) ΔH>0, 某温度下,向5 L密闭容器中加入2 mol C(s)与1 mol H2O(g),t1 s时,CO的物质的量为0.20 mol,到第t2 s时恰好达到平衡,此时CO的物质的量为0.35 mol ,下列说法正确的是( )
CO(g)+H2 (g) ΔH>0, 某温度下,向5 L密闭容器中加入2 mol C(s)与1 mol H2O(g),t1 s时,CO的物质的量为0.20 mol,到第t2 s时恰好达到平衡,此时CO的物质的量为0.35 mol ,下列说法正确的是( )
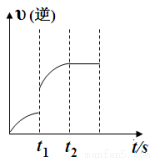
A. t1时改变的条件可能是使用催化剂
B.t1时改变的条件可能是增大 H2O 浓度
C.t1~t2这段时间内的化学反应速率 v(H2O)= 0.15/(t2-t1)
D.t2后继续加入 2 mol C(s)平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:选择题
下列各组反应中关于能量的比较正确的是( )
①H2(g)+Cl2(g)=2HCl(g)△H1;
1/2H2(g)+1/2Cl2(g)=HCl(g)△H2;△H1>△H2
②2H2O(l)=2H2(g)+O2(g)△H1;
2Na(s)+2H2O(l)=2NaOH(aq)+H2(g)ΔH2;△H1>△H2
③CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(l)△H1;
CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(g)△H2;△H1<△H2
④t ℃时,在一定条件下,将 1 mol N2和 3 mol H2 分别置于恒容和恒压的两个密闭容器中,达到平衡状态时放出的热量分别为 Q1、Q2;Q1<Q2
A.①③④ B.①②④ C.②③④ D.①③
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二上期中化学卷(解析版) 题型:选择题
常温下,下列各组物质中,Y既能与X反应又能与Z反应的是
X | Y | Z | |
① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
② | KOH溶液液 | Na2CO3 | 稀盐酸 |
③ | CO2 | Na2O2 | H2O |
④ | FeCl3溶液 | Cu | 稀硫酸 |
A.①③ B.①④ C.②④ D.②③
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二上期中化学卷(解析版) 题型:选择题
下列关于NaHCO3的说法正确的是
A.俗名是苏打或纯碱 B.同温度时的溶解度比Na2CO3大
C.与盐酸反应时比Na2CO3快 D.热稳定性强,受热难以分解
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一上期中化学卷(解析版) 题型:实验题
碘化钠是实验室中常用的分析试剂,工业上用铁屑还原法制备NaI的流程如图所示。

请回答下列问题:
(1)判断反应①中碘是否反应完全的方法是 。
(2)操作Ⅰ的名称是 。
(3)反应①的化学方程式为 。
(4)反应②中NaIO3被Fe单质还原为NaI,同时生成Fe(OH)3,写出该反应的化学方程式并用双线桥法表示此反应的电子转移的方向及数目
(5)在反应②中若有99 g NaIO3被还原,则转移电子的物质的量为 mol。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高一上期中化学试卷(解析版) 题型:选择题
在下列变化中,需要加入合适的氧化剂才能实现的是( )
A.HCl→H2 B.CO2→CO C.FeCl3→FeCl2 D.SO2→SO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com