
����Ŀ��Ӧ������װ�ã���Ӳ�ʲ������з��뻹ԭ���ۺ�ʯ���Ļ������ȣ���ͨ��ˮ�������Ϳ�����ɸ�����"Fe��ˮ������Ӧ��ʵ��"��
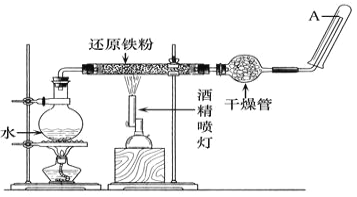
��ش��ʵ���е����⡣
��1��ʵ��ǰ���������װ�ý��������Եļ�飬����������_____________��
��2��Բ����ƿ��ʢװ����ˮ����װ�����Ⱥ����Ҫ������_______________����ƿ�ײ������˼�Ƭ���Ƭ�����Ƭ��������_______________��
��3���ƾ��ƺ;ƾ���Ƶ�ȼ��˳����__________��
��4���������ʢװ�����ʿ�����_____________��������__________��
��5�����Ҫ��A�������ܿڴ���ȼ�����壬�����Ը��������_________����һ������Ŀ��_____��
���𰸡��������ĩ�˵ĵ���A����ˮ�У��þƾ��ƻ�������ƿ�ײ�������ܹ۲쵽����ˮ�еIJ������ܿ�������ð����ֹͣ���Ⱥ�����������ˮ���������ҽϳ�ʱ�䲻���䣬���������װ�õ����������á� ΪӲ�ʲ�������Fe��ˮ�����ķ�Ӧʵ���ṩ�������ϵ�ˮ���� ��ֹ���� �ȵ�ȼ�ƾ��ƣ�����ˮ�������ٵ�ȼ�ƾ���� ��ʯ�� ��ȥ����H2�е�ˮ���� �鴿 ��ֹH2������������ը
��������
��1������װ�������Եķ���һ�����ȵķ���������ð�������ݺͻ�����ˮ�����жϣ�
��2����Ӧ��Ϊˮ���������������Ƭ��Ŀ���Ƿ�ֹ�����¹ʷ�����
��3�������һ��װ������Ҫ�������ȣ�һ��Ҫע���ȼ����������˳��һ���Ǹ���ʵ��İ�ȫ�ԺͶ�ʵ������Ӱ�������ǣ�
��4���������������������ã�ʢ�Ź���������
��5����ȼ����ǰһ��Ҫ���鴿�ȣ���ֹ������ը��
��1����ѧ�μ��װ�������Գ��÷��������֣�һ����������������ԭ������һ����������ѹԭ������ѹԭ��һ��ֻ���漰��Һ��ʱ�����õõ���������Ȼ��������������ԭ����������������ԭ��ʱҪע�ⲽ��һ��Ҫ��������Ҫ֤�������͡���ҲҪ֤�������������ʲ�������Ϊ���������ĩ�˵ĵ���A����ˮ�У��þƾ��ƻ�������ƿ�ײ�������ܹ۲쵽����ˮ�еIJ������ܿ�������ð����ֹͣ���Ⱥ�����������ˮ���������ҽϳ�ʱ�䲻���䣬���������װ�õ����������ã�
��2����Ϊ��Ӧ��Ϊˮ��������������Բ����ƿ��ʢװ����ˮ����װ�����Ⱥ����Ҫ������ΪӲ�ʲ�������Fe��ˮ�����ķ�Ӧʵ���ṩ�������ϵ�ˮ��������ƿ�ײ�Ӧ���ȷ������Ƭ�������Ƭ��Ŀ���Ƿ�ֹ�����¹ʷ�����
��3����ȼ����������˳��Ҫ����ʵ��İ�ȫ�ԺͶ�ʵ������Ӱ�죬�ڱ�ʵ����Ϊ�˷�ֹ��������е������ڼ�ǿ�ȵ������·�Ӧ��Ӧ���ȵ�ȼ�ƾ��ƣ����ƾ��ƺ;ƾ���Ƶ�ȼ��˳�����ȵ�ȼ�ƾ��ƣ�����ˮ�������ٵ�ȼ�ƾ���ƣ�
��4���������ʢװ�ǵ������Ǽ�ʯ�ң������dz�ȥ��Ӧ�����������е�ˮ������
��5�������ı�ը������4.0%��75.6%������˵�������ĺ�����������Χ�ڵĻ��ͻ�����ը����ˣ���ȼ֮ǰҪ���鴿�ȣ�Ŀ���Ƿ�ֹH2������������ը��


 ��ʦ�㲦��ϵ�д�
��ʦ�㲦��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͬ�ĵ��Ӳ�ṹ����������aAn+��bB(n+1)+��cCn-��dD(n+1)-������A��B��C��D����Ԫ��������ȷ����
A.һ�����Ƕ�����Ԫ��
B.ԭ��������B > A > C > D
C.���ʵĻ�ԭ�ԣ�B > A
D.��̬�⻯����ȶ��ԣ�D > C
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��������γ�ʾ��ͼ������ͼʾ�ش��������⡣
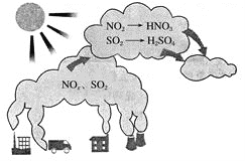
��1����������������������_____��
A��CO2 B��SO2 C��N2 D��NO2
��2��������ˮ��Ʒ1�ݣ�ÿ��һ��ʱ��ⶨ����ˮ��Ʒ��pH�������������£�
����ʱ��/h | 0 | 1 | 2 | 3 | 4 |
��ˮ��pH | 4.73 | 4.63 | 4.56 | 4.55 | 4.55 |
�������ݣ��ش��������⣺
����ˮ��Ʒ��pH�仯��ԭ����____(�û�ѧ����ʽ��ʾ)��
���������ȡ����������ˮ������ˮ���ϣ�pH����____��ԭ����_____(�û�ѧ����ʽ��ʾ)��
��3�����д�ʩ�У��ɼ������������;������____(����ĸ)��
������ú��ȼ�� �ڰѹ����̴���� ��ȼ������ �������ữ�������м�ʯ�� �ݿ�������Դ
A���٢ڢ� B���ڢۢܢ� C���٢ۢ� D���٢ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����п�ͼ�漰����������Ԫ���У���һ��Ԫ���⣬�����Ϊ1��18��Ԫ�ء�
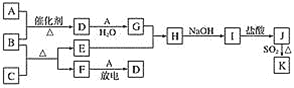
��֪��A��FΪ��ɫ���嵥�ʣ�BΪ���д̼�����ζ�����壬��ѧ�ҹ�����ϳ�B���1918���ŵ������ѧ����CΪ��ɫ�����EΪ�Ϻ�ɫ�������ʣ�IΪ��ɫ����(���ַ�Ӧ�IJ���δ�г�)����ش��������⣺
(1)������������G��Ũ��Һ������γ�һ�����ܵı���Ĥ���������Ϊ___________��
(2)E��G��ϡ��Һ��Ӧ�����ӷ���ʽΪ_________��
(3)��25 ���101 kPa�������£���VL��B��������100 mLˮ�У��õ��ܶ�Ϊ��g��mL��1����ҺM����M��Һ�����ʵ���Ũ��Ϊ________ mol��L��1��(��֪25 �桢101 kPa����������Ħ�����Ϊ24.5 L��mol��1�����ػ���)
(4)�ֱ�պȡB��Ũ��Һ��G��Ũ��Һ�IJ��������ӽ����������_________��
(5)B��C��Ӧ�Ļ�ѧ����ʽΪ__________��
(6)J��K��ͬ�ֽ����IJ�ͬ�Ȼ��KΪ��ɫ������д��SO2��ԭJ����K�����ӷ���ʽ��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�ɷֱ�ͨ������������Ӧ��ȡ����: �� ��
a.CH3CH2OH(g)+H2O(g) ![]() 4H2(g)+2CO(g)����H=+256.6 kJ��mol-1
4H2(g)+2CO(g)����H=+256.6 kJ��mol-1
b.2CH3CH2OH(g)+O2(g) ![]() 6H2(g)+4CO(g)����H=+27.6 kJ��mol-1
6H2(g)+4CO(g)����H=+27.6 kJ��mol-1
������˵����ȷ���ǣ� ��
A.�Ҵ���ȼ������H=-13.8 kJ��mol-1
B.���߷�Ӧa�ķ�Ӧ�¶ȣ��Ҵ���ת���ʼ�С
C.2H2(g)+O2(g)=2H2O(g)����H=-229 kJ��mol-1
D.��ȡ��������������Ӧb���յ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������·�Ӧ��2A��g��+B��g��![]() 3C��g�� ��H��0���ں��ݵ��ܱ������дﵽƽ��������ı�ͼ�к�����x��ֵ�����´ﵽƽ���������y��x�仯���ƺ�������
3C��g�� ��H��0���ں��ݵ��ܱ������дﵽƽ��������ı�ͼ�к�����x��ֵ�����´ﵽƽ���������y��x�仯���ƺ�������
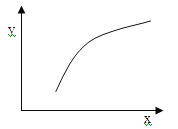
ѡ�� | x | y |
A | A��Ũ�� | ƽ�ⳣ��K |
B | �¶� | ���������ܶ� |
C | B�����ʵ��� | A��ת���� |
D | ���������� | C��������� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijϡ��Һ�к���Fe(NO3)3��Cu(NO3)2��HNO3���������������ۣ���Һ��Fe2+Ũ�Ⱥͼ������۵����ʵ����Ĺ�ϵ��ͼ��ʾ��
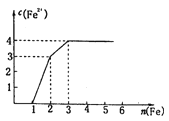
��Һ��Fe(NO3)3��Cu(NO3)2��HNO3���ʵ���Ũ��֮��Ϊ
A.1:1:1B.1:3:1C.1:1:4D.3:3:8
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ���仯�����ڹ�ҵ��������������;��ij�����Ի�ͭ��(��Ҫ�ɷ�Ϊ Cu2S�������� Fe2O3��SiO2 ������)Ϊԭ���Ʊ�������ˮ�ļ�ʽ̼��ͭ���������£�
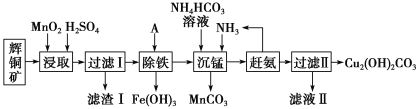
��֪��
�ٳ����¼������ʿ�ʼ�γɳ�������ȫ����ʱ��pH���±�
�������� | Fe2�� | Fe3�� | Cu2�� | Mn2�� |
��ʼ���� | 7.5 | 2.7 | 5.6 | 8.3 |
��ȫ���� | 9.0 | 3.7 | 6.7 | 9.8 |
�� Ksp[Fe(OH)3]��4.0��10��38
(1)�ӿ�����ȡ�����ʣ����ʵ���������Ũ���⣬���ɲ�ȡ�Ĵ�ʩ��__________����дһ�֣���
(2)����I�е���Ҫ�ɷ���MnO2��S��SiO2����д������ȡ����Ӧ������S�Ļ�ѧ����ʽ��______________��
(3)��������������ʱ������Լ�A����CuO�ȣ�����pH���ķ�ΧΪ_________������ A ����Һ�� pH��Ϊ4.0������Һ�� Fe3����Ũ��Ϊ_________mol/L��
(4)д����������(�� Mn2��)�����з�Ӧ�����ӷ���ʽ��_________________________��
(5)���ϰ���ʱ�������˵IJ���������________________��
(6)���ˢ�õ��ij�������ϴ�ӡ�������Եõ���ʽ̼��ͭ���жϳ����Ƿ�ϴ���IJ�����________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com