
| A. | 0.01g | B. | 0.02g | C. | 0.14g | D. | 0.17g |
分析 根据氢氧化钠计算剩余的硫酸,进而计算与氨气反应的硫酸的物质的量,再根据关系式2N~2NH3~H2SO4计算氮元素的质量;
解答 解:令40mL1.00mol•L-1的 NaOH溶液中和硫酸的物质的量为n,则:
2NaOH+H2SO4=Na2SO4+2H2O
2 1
0.04L×1mol/L n
解得:n=0.040L×1mol/L×$\frac{1}{2}$=0.02mol
故吸收氨气的硫酸的物质的量为:0.500mol•L-1×0.05mL-0.02mol=0.005mol
令20.0mL牛奶中氮元素的质量是m,则:
2N~2NH3~H2SO4
28g 1mol
m 0.005mol
所以m=28g×$\frac{0.005mol}{1mol}$=0.14g
故选C.
点评 本题考查根据方程式的计算、质量分数的有关计算,难度不大,根据N元素守恒确定蛋白质中氮元素与硫酸反应的关系式是解题关键.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大容器体积 | B. | 通入大量O2 | C. | 移去部分SO2 | D. | 降低体系温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
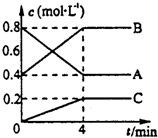 一定条件下,A、B、C三种气体在绝热密闭容器中随反应进行,温度升高;且各物质浓度的变化情况如图所示,通过分析回答:
一定条件下,A、B、C三种气体在绝热密闭容器中随反应进行,温度升高;且各物质浓度的变化情况如图所示,通过分析回答:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
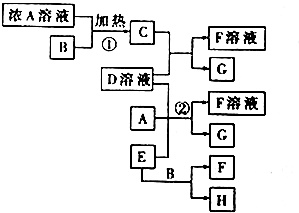
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 磺化煤能使具有永久硬度的水软化,因为它能除去水中的Ca2+、Mg2+、SO42-和Cl-等 | |
| B. | 经磺化煤软化处理后,软水中Na+浓度增大 | |
| C. | 磺化煤使硬水软化以及磺化煤的再生,这两种操作可以在同一离子交换柱中同时进行 | |
| D. | 失去软化硬水能力的磺化煤,不可能恢复它的软化能力 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com