
| A、Na+、K+、SO42-、Cl- |
| B、Fe2+、H+、SO42-、NO3- |
| C、H+、K+、HCO3-、Cl- |
| D、Mg2+、Na+、Cl-、SO42- |


科目:高中化学 来源: 题型:
| A、增大NO2或CO的浓度 |
| B、减小CO2或NO的浓度 |
| C、通入Ne使气体的压强增大 |
| D、升高反应的温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等体积、等浓度的Ba(OH)2溶液与KAl(SO4)2溶液混合:3Ba2++6OH-+2 Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ |
| B、向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
| C、Fe3O4与稀硝酸反应的离子方程式为:Fe3O4+8H+═Fe2++2Fe3++4H2O |
| D、向NaOH溶液中加入金属铝:Al+2OH-═AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜铸塑像上出现铜绿[Cu2(0H)2C03] |
| B、用石膏点豆腐 |
| C、不良商贩用硫黄熏蒸法制作“白豆芽” |
| D、自来水厂用氯气对水进行消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5 mol |
| B、1 mol |
| C、2 mol |
| D、4 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①=③>② |
| B、③>②>① |
| C、③=②>① |
| D、①=②=③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O |
| B、Na2O2 |
| C、Na2O和Na2O2 |
| D、Na2O2和NaO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
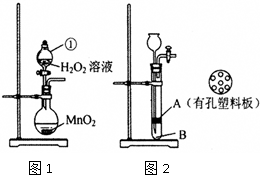
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com