
(12分)物质结构选修模块题
(1)已知:常压下,氨气在300℃时约有9.7%分解,水蒸气在2000℃时约有4%分解,氟化氢气体在3000℃时仍不分解。这三种分子的中心原子与氢原子形成的σ键能由大到小的顺序是 ;其中水分子里的氧原子轨道的杂化类型是 。将过量氨气通入0.1 mol·L―1的蓝色硫酸铜溶液中逐渐形成深蓝色溶液,其离子方程式为: 。
(2)用钛锰储氢合金储氢,与高压氢气钢瓶相比,具有重量轻、体积小的优点。下图是金属钛的面心立方结构晶胞示意图,则钛晶体的1个晶胞中钛原子数为 ,钛原子的配位数为 。

(3)晶体硅、锗是良好的半导体材料。磷化铝、砷化镓也是重要的半导体材料,从物质结构的角度分析它们与晶体硅的关系为 。试以原子实的形式写出31号半导体元素镓的电子排布式 。镓与砷相比较,第一电离能更大的是 (用元素符号表示)。
(12分,每空2分)HF>H2O>NH3或HF>HO>NH(2分) sp3(1分)
Cu2++ 4NH3=[Cu(NH3 )4]2+(2分)(2) 4(1分) 12(1分)
(3)等电子体(2分) [Ar]3d104s24p1 (2分,氩原子实写全也给分) As(1分)
【解析】
试题分析:(1)已知:常压下,氨气在300℃时约有9.7%分解,水蒸气在2000℃时约有4%分解,氟化氢气体在3000℃时仍不分解,这说明H—F键能最强。非金属性越强,与氢元素形成的共价键越牢固,则这三种分子的中心原子与氢原子形成的σ键能由大到小的顺序是HF>H2O>NH3;其中水分子里的氧原子含有2对孤对电子,价层电子对数是4,则氧原子对轨道的杂化类型是 sp3。铜离子能与氨气形成配位健,则将过量氨气通入0.1 mol·L―1的蓝色硫酸铜溶液中逐渐形成深蓝色溶液的离子方程式为Cu2++ 4NH3=[Cu(NH3 )4]2+。
(2)根据金属钛的面心立方结构晶胞示意图可知,钛晶体的1个晶胞中钛原子数为 。以晶胞的顶点为中心可判断钛原子的配位数为
。以晶胞的顶点为中心可判断钛原子的配位数为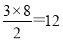 。
。
(3)互为等电子体的物质结构与性质相似,则从物质结构的角度分析它们与晶体硅的关系为等电子体。根据核外电子排布规律可知31号半导体元素镓的电子排布式为[Ar]3d104s24p1。非金属性越强,第一电离能越大。但砷元素的4p轨道电子处于半充满状态,稳定性强,则镓与砷相比较,第一电离能更大的是As。
考点:考查共价键、配位健、晶胞结构以及核外电子排布等


科目:高中化学 来源:2014-2015河南省濮阳市高二上学期第三次月考化学试卷(解析版) 题型:选择题
对于密闭容器中进行的反应CO(g) + H2O(g) CO2 (g) +H2 (g),达到平衡后,其他条件不变,增大CO的浓度,下列说法不正确的是
CO2 (g) +H2 (g),达到平衡后,其他条件不变,增大CO的浓度,下列说法不正确的是
A.正反应速率增大
B.逆反应速率减小
C.达到平衡时,逆反应速率比原平衡要大
D.化学平衡常数不变
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省景德镇市高三第二次质检理综化学试卷(解析版) 题型:填空题
(12分)
Ⅰ、按要求写出下列反应的方程式:
(1)碳酸氢铵与少量的氢氧化钠溶液反应(离子方程式) 。
(2)氯化铁溶液中通入二氧化硫气体(离子方程式) 。
(3)一定量的硫酸铝钾加入氢氧化钡溶液生成沉淀质量最大时的反应(化学方程式) 。
(4)碘化亚铁和氯气以5:7的物质的量比反应(化学方程式) 。
Ⅱ、已知Fe2O3在高炉中有下列反应:Fe2O3+CO=2FeO+CO2,反应形成的固体混合物(Fe2O3和FeO)中,元素铁和氧的质量比用m(Fe):m(O)表示。
(1)上述固体混合物中,m(Fe):m(O)可能是 。
a.7:5 b.3:1 c.7:1
(2)设Fe2O3被CO还原的百分率为A%,则用含m(Fe)、m(O)的代数式表示A%的关系式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省镇江市高三第一学期期末调研测试化学试卷(解析版) 题型:选择题
化合物Ⅲ是合成中药黄芩中的主要活性成分的中间体,合成方法如下:

下列有关叙述正确的是
A.I在空气中能稳定存在
B.II中所有原子均有可能共面
C.可用FeCl3溶液鉴别有机物II和III
D.1mol产物III与足量溴水反应,消耗Br2的物质的量为1.5mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省镇江市高三第一学期期末调研测试化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列说法正确的是
A.1mol甲醇中含有C—H键的数目为4NA
B.常温下,2.24LCl2完全与NaOH溶液反应,转移的电子数目一定为0.1 NA
C.7.8g由Na2S和Na2O2组成的混合物中含有阴离子的数目为 0.1NA
D.80℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2 NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省苏州市高三上学期期末调研测试化学试卷(解析版) 题型:填空题
(12分)继侯德榜“联合制碱法”后,上世纪50年代某些化工专家开始研究有机胺制碱法,目前这项研究工作取得了一定进展。其工艺流程如下:

已知:NR3+ HC=NR3 HCl,且NR3 HCl易溶于有机溶剂。
(1)有机胺制碱法反应生成小苏打的化学方程式是: ;操作①称为 ;
(2)过程③得到产品的化学方程式是: ;
(3)在过程④中,回收有机胺的化学方程式是: ;
(4)副产品的用途 ;
(5)本工艺流程中可循环利用的物质是: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省苏州市高三上学期期末调研测试化学试卷(解析版) 题型:选择题
下图为“长式元素周期表”的一部分,其中短周期元素W、X、Y、Z的位置关系如图。下列说法一定正确的是

A.元素Z位于元素周期表的第3周期ⅦA族
B.原子半径的大小顺序为:rY>rW>rX
C.元素W的最高价氧化物对应水化物的酸性比Y的强
D.元素X的气态简单氢化物的热稳定性比W的强
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省郴州市高三第二次月考理综化学试卷(解析版) 题型:选择题
下列各组离子能在指定环境中大量共存的是:
A.在c(HCO3-)=0.1 mol.L-1的溶液中:NH4+、AlO2—、Cl-、NO3—
B.在由水电离出的c(H+)=l×l0-12 ·mol.L-1的溶液中:Fe2+、ClO-、Na+、SO42-
C.在加入铝粉产生H2的溶液中:SO42-、NO3一、Na+、NH4+
D.在使红色石蕊试纸变蓝的溶液中:SO32-、CO32-、Na+、F—
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州市高三上学期期末化学试卷(解析版) 题型:简答题
(11分)根据物质相似性、特殊性来学习元素性质是常见的学习方法。
(1)铍(Be)与铝元素相似,其氧化物及氢氧化物具有两性,请写出BeO与盐酸反应的离子方程式_____,Be(OH)2溶于NaOH溶液的化学方程式为:Be(OH)2+2NaOH=Na2 BeO2+2H2 O,往10.0mL1.00mol·L-1的Be(NO3)2溶液中逐滴加入等浓度的NaOH溶液,请在以下坐标图中画出沉淀量随NaOH溶液加人量的变化图:

(2)锗与硅元素相似,锗也是良好的半导体,以下是工业冶炼锗的简单流程图:

①GeCl4的晶体类型为__________。
②写出过程III发生反应的化学方程式__________。
③以下有关工业冶炼锗的说法正确的是__________。
A.GeO2与SiO2性质相似,均易与盐酸反应
B.过程II的蒸馏是利用GeCl4难溶于水的性质实现的
C.过程IV发生的反应中,GeO2作氧化剂
D.上述过程涉及的基本反应类型有复分解反应、置换反应
(3)某同学为了探究硫与浓硝酸的反应产物,将硫与浓硝酸混合,结果生成一种纯净无色气体A,A遇空气变红棕色,据此写出硫与浓硝酸反应的化学方程式___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com