
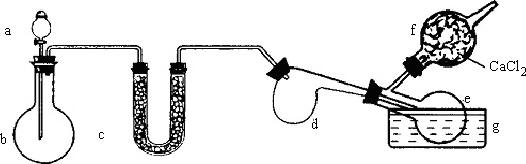
用下图装置(酒精灯、铁架台等未画)制取三氯化磷,在曲颈甑d中放入足量白磷,将![]() 迅速而不间断地通入曲颈甑中,
迅速而不间断地通入曲颈甑中,![]() 与白磷就发生反应,产生火焰.
与白磷就发生反应,产生火焰.
![]() 和
和![]() 熔点分别是-112℃,148℃,沸点分别是76℃,200℃.
熔点分别是-112℃,148℃,沸点分别是76℃,200℃.
(1)现有浓盐酸、浓硫酸、白磷、二氧化锰、氢氧化钠供选用,a、b中应装入的试剂分别为:a_________,b__________.
(2)需加热的仪器是________(填仪器字母).
(3)生成的![]() 在e中收集,为保证
在e中收集,为保证![]() 蒸气冷凝,应在水槽g中加入________.
蒸气冷凝,应在水槽g中加入________.
(4)![]() 遇到水蒸气强烈反应,甚至爆炸,所以d、e仪器及装入的物质都不能含有水.为除去氯气中的水分,c可装入的物质是________.
遇到水蒸气强烈反应,甚至爆炸,所以d、e仪器及装入的物质都不能含有水.为除去氯气中的水分,c可装入的物质是________.
A.碱石灰 B.浓硫酸 C.无水氯化钙
(5)氯气和白磷反应放出大量的热,为使曲颈甑d不致因局部过热而炸裂,实验开始前应在曲颈甑底部放少量____________.
(6)实验室白磷保存在水中,取出白磷后用滤纸吸干表面水分,浸入无水乙醇中片刻,再浸入乙醚中片刻即可完全除去水分.已知水与乙醇互溶,用上述方法除水分的原因是________________________________________________.
(7)为防止氯气污染空气,装置末端导出的气体最好用________进行净化处理.
[ ]
A.![]() 溶液 B.
溶液 B.![]() 溶液 C.饱和食盐水
溶液 C.饱和食盐水
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:阅读理解

| 实 实验过程 | 实验现象 | 有关化学方程式 | ||||||||||||||||
| 在C中加入样品标本W克,D中装入药品后并称量为m1克.连接好仪器后,检查气密性 | B、E中有气泡产生 B、E中有气泡产生 |
2H2O2
2H2O2
| ||||||||||||||||
| 打开A的活塞,慢慢滴加溶液. | C中的红褐色粉末变成黑色 C中的红褐色粉末变成黑色 |
2Cu+O2
2Cu+O2
| ||||||||||||||||
| 对C进行加热.当C中药品充分反应后.关闭A的活塞.停止加热: | 无 无 |
无 无 | ||||||||||||||||
| 冷却后,称量D的质量为m2克. | 无 无 |
无 无 |
W-(m2-m1)×
| ||
| W |
W-(m2-m1)×
| ||
| W |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2015届江西省抚州市高一下学期期末考试化学试卷(解析版) 题型:实验题
乙烯是来自石油的重要有机化工原料,其产量通常用来衡量一个国家的石油化工发展水平。结合以下路线回答:

已知:
(1)反应II的化学方程式是 。
(2)D为高分子化合物,可以用来制造多种包装材料,其结构简式是 。
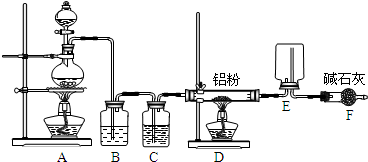
(3)E是有香味的物质,在实验室用下图装置制取。

①反应IV的化学方程式是 ,该反应类型为 。
②该装置图中有一个明显的错误是 。
(4)为了证明浓硫酸在反应IV中起到了催化剂和吸水剂的作用,某同学利用上图改进后装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管乙再测有机层的厚度,实验记录如下:
实验编号 试管甲中试剂 试管乙中试剂 有机层的厚度/cm
A 2 mL乙醇、1 mL乙酸、
1mL18mol·L-1 浓硫酸 饱和Na2CO3溶液 3.0
B 2 mL乙醇、1 mL乙酸 0.1
C 2 mL乙醇、1 mL乙酸、
3 mL 2mol·L-1 H2SO4 0.6
D 2 mL乙醇、1 mL乙酸、盐酸 0.6
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是3mL和 mol·L-1 。
②分析实验 (填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率。
查看答案和解析>>
科目:高中化学 来源:2012届甘肃省高二下学期期中考试化学试卷 题型:实验题
(12分) 某实验小组用下图装置进行乙醇催化氧化的实验。[来源:学.科.网Z.X.X.K]
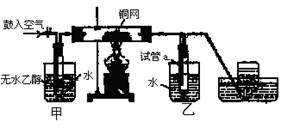
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式 。
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是 反应(放热或吸热)。
(2)甲和乙两个水浴作用不相同。甲的作用是 ;
乙的作用是 。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是 ,
集气瓶中收集到的气体的主要成分是 。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有 。要除去该物质,可先在混合液中加入 (填写字母)。然后,再通过 (填实验操作名称)即可除去。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com