
| A. | 用氨水鉴别MgCl2溶液和AlCl3溶液 | |
| B. | 用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液 | |
| C. | 用AgNO3鉴别Na2CO3溶液和NaCl溶液 | |
| D. | 用足量的盐酸和BaCl2溶液鉴别溶液中是否含SO42- |
分析 A.二者均与氨水反应生成白色沉淀;
B.二者均与石灰水反应生成白色沉淀;
C.二者均与硝酸银反应生成白色沉淀;
D.先加盐酸排除干扰离子,再加氯化钡观察是否生成白色沉淀.
解答 解:A.二者均与氨水反应生成白色沉淀,现象相同,不能鉴别,故A不选;
B.二者均与石灰水反应生成白色沉淀,现象相同,不能鉴别,故B不选;
C.二者均与硝酸银反应生成白色沉淀,现象相同,不能鉴别,故C不选;
D.先加盐酸排除干扰离子,再加氯化钡观察是否生成白色沉淀,若生成白色沉淀,则含SO42-,反之不含,故D选;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质性质、物质鉴别、离子检验为解答的关键,侧重分析与实验能力的考查,注意实验与元素化合物知识的结合,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠加入到紫色石蕊试液中,紫色石蕊先变红后褪色且有气泡产生 | |
| B. | 冷的浓硫酸和浓硝酸都可以用铝、铁的容器盛装 | |
| C. | 硅、氯、硫、氮、钠元素在自然界只有化合态没有游离态 | |
| D. | 浓硝酸有氧化性,稀硝酸没有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时PbO2发生氧化反应 | |
| B. | 充电时电解质溶液的质量减少 | |
| C. | 放电时的负极反应式为Pb+SO42--2e-=PbSO4 | |
| D. | 充电时的阴极反应式为PbSO4+2H2O-2e-=PbO2+SO42-+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 实验内容 | 实验目的 |
| A | 向含有酚酞的Na2CO3溶液中加入少量BaC12固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| B | 室温下,用pH试纸分别测定浓度为18mol/L和0.1mol/L H2SO4溶液的pH | 比较不同浓度H2SO4的酸性强弱 |
| C | 配制FeCl2溶液时,先将FeCl2溶于适量浓盐酸中,再用蒸馏水稀释到所需浓度,最后在试剂瓶中加入少量铜粉 | 抑制Fe2+水解,并防止Fe2+被氧化 |
| D | 向10mL 0.2mol/L NaOH溶液中滴入2滴0.1mol/LMgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/LFeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下的Ksp>Ksp |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
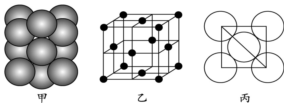 已知 X、Y、Z、Q、R、E六种前四周期元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如表.
已知 X、Y、Z、Q、R、E六种前四周期元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如表.| 元素 | 结构或性质信息 |
| X | 原子的L层上s电子数等于p电子数 |
| Y | 原子核外的L层有3个未成对电子 |
| Z | 地壳中含量最多的元素 |
| Q | 单质常温常压下是气体,原子的M层上有1个未成对的p电子 |
| R | 核电荷数是Y与Q的核电荷数之和 |
| E | N能层上只有一个电子,K、L、M层均排满电子 |
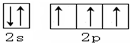 .X的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为3:2.
.X的一种氢化物相对分子质量为26,其分子中的σ键与π键的键数之比为3:2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | |||||
| Z | Y | M | N |
| A. | N的氧化物对应水化物的酸性一定比X的氧化物对应水化物的酸性强 | |
| B. | 相同条件下,与同浓度、同体积的盐酸反应,单质Z的反应速率大于单质Y | |
| C. | X的原子半径比Y的小 | |
| D. | X和M的原子序数相差10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核素23Na的中子数是12 | |
| B. | 16O和18O互为同位素 | |
| C. | 电离方程式:CH3COOH?CH3COOˉ+H+ | |
| D. | 16O、1H、2H、3H四种核素可构成4种水分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ①③⑤⑦ | C. | ④⑧ | D. | ②④⑥⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com