
分析 n(CO2)=$\frac{16.8L}{22.4L/mol}$=0.75mol,n(NaOH)=1mol/L×1L=1mol,利用Na、C原子守恒列方程式组进行计算.
解答 解:n(CO2)=$\frac{16.8L}{22.4L/mol}$=0.75mol,n(NaOH)=1mol/L×1L=1mol,设NaHCO3和Na2CO3的物质的量分别是xmol、ymol,利用Na、C原子守恒列方程式组得:
$\left\{\begin{array}{l}{x+2y=1}\\{x+y=0.75}\end{array}\right.$
解得$\left\{\begin{array}{l}{x=0.5}\\{y=0.25}\end{array}\right.$,
答:溶液中含有NaHCO3和Na2CO3的物质的量分别是0.5mol、0.25mol.
点评 本题考查混合物的有关计算,侧重考查分析计算能力,利用原子守恒分析解答即可,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
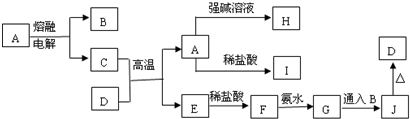
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,A的结构式为
,A的结构式为 ,A分子的空间构型是三角锥形.
,A分子的空间构型是三角锥形.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
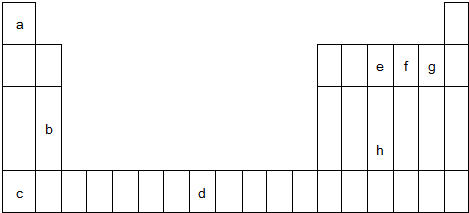
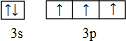 ;
;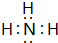 ,其分子的空间构型是三角锥形,分子中e原子的杂化类型是sp3.
,其分子的空间构型是三角锥形,分子中e原子的杂化类型是sp3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
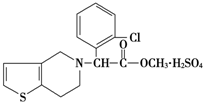 波立维是国家刚刚引进的新药,它给中风、心肌梗死等心脏病患者带来福音,波立维属于硫酸氢盐,它的结构如图所示,下列关于它的说法正确的是( )
波立维是国家刚刚引进的新药,它给中风、心肌梗死等心脏病患者带来福音,波立维属于硫酸氢盐,它的结构如图所示,下列关于它的说法正确的是( )| A. | 该物质的化学式为C16H15ClNO2•H2SO4 | |
| B. | 该物质难溶于水 | |
| C. | 波立维能形成硫酸氢盐是与其结构中的氮原子有关 | |
| D. | 它可以与NaOH溶液反应,1 mol该物质最多可消耗2mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种阳离子 | B. | 一种单质和一种化合物分子 | ||
| C. | 一种分子和一种离子 | D. | 一种原子和一种分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com