
下表所列各组物质中,不能通过一步反应实现如图所示转化的是( )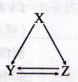
| 选项 | X | Y | Z |
| A | AlCl3 | Al(OH)3 | NaAlO2 |
| B | C | CO | CO2 |
| C | CH2=CH2 | CH3CH2Br | CH3CH2OH |
| D | S | SO2 | SO3 |
D
解析试题分析:采用选项代入法结合相关元素单质及其化合物的性质和相互转化关系解答。A、AlCl3与适量NaOH反应可生成Al(OH)3,与过量NaOH反应可生成NaAlO2,Al(OH)3与NaOH反应可生成NaAlO2,NaAlO2与盐酸反应可生成Al(OH)3,可以通过一步反应实现,错误;B、C与少量O2反应可生成CO,与过量O2反应可生成CO2,CO与O2反应可生成CO2,CO2与C反应可生成CO,可以通过一步反应实现,错误;C、CH2=CH2与水加成生成CH3CH2OH,与HBr加成生成CH3CH2Br,CH3CH2OH与氢溴酸发生取代反应可生成CH3CH2Br,CH3CH2Br发生水解反应可生成CH3CH2OH,可以通过一步反应实现,错误;D、S不能通过一步反应生成SO3,正确。
考点:考查无机物的推断及相关元素单质及其化合物的性质和相互转化关系


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:实验题
某兴趣小组研究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示: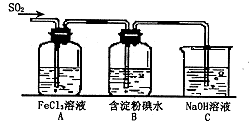
(1)SO2气体与Fe3+反应的主要产物是____、 。(填离子符号)
(2)下列实验方案可以用于在实验室制取所需SO2的是 。
| A.Na2SO3溶液与HNO3 | B.Na2SO3固体与浓硫酸 |
| C.固体硫在纯氧中燃烧 | D.铜与热浓H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化合物A、B、C、D各由两种元素组成,甲、乙、丙是短周期元素的三种单质。这些常见的化合物与单质之间存在如下关系(已知C是一种有机物),以下结论不正确的( )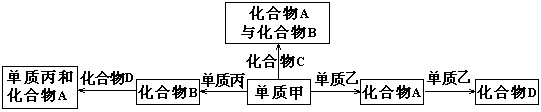
A.常温下,化合物A、B、C、D均为气体
B.上图所示的五个转化关系中,有三个是化合反应
C.上图所示的五个转化关系中,均为氧化还原反应
D.上述转化关系所涉及的化合物中只有一种是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合下图。则甲和X(要求甲和X互换后也能符合要求)是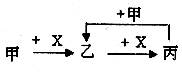
①Na2CO3溶液和稀盐酸;②Cl2和Fe;③C和O2;④SO2和NaOH溶液;⑤AlCl3溶液和NaOH溶液
| A.①②③④均可以 | B.②③④⑤均可以 |
| C.①②③⑤均可以 | D.①③④⑤均可以 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
A~E是中学常见的5种化合物,A、B是氧化物,它们之间的转化关系如下图所示。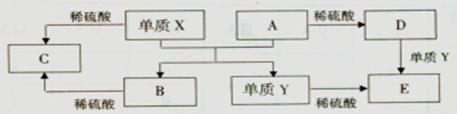
则下列说法正确的是( )
A.x与A反应的化学方程式是:
B.检验D溶液中的金属阳离子的反应:Fe3++3SCN—= Fe(SCN)3↓
C.单质Y在一定条件下能与水发生置换反应
D.由于化合物B和C均既能与酸反应,又能与碱反应,所以均是两性化合物
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
A~E是中学常见的5种化合物,A、B是氧化物,它们之间的转化关系如下图所示。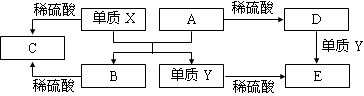
则下列说法正确的是
A.X与A反应的化学方程式是:Al2O3 + 2Fe Fe2O3 + 2Al
Fe2O3 + 2Al
B.检验D溶液中的金属阳离子的反应:Fe3++3SCN—=Fe(SCN)3↓
C.单质Y在一定条件下能与水发生置换反应
D.由于化合物B和C均既能与酸反应,又能与碱反应,所以均是两性化合物
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题: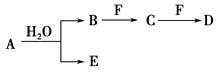
(1)若常温下A为有色气体。
①当F是一种金属单质时,请写出一定浓度的B溶液和适量F反应生成C与气体E的离子方程式:______________________________________________。
②当C为直线形分子时,E具有漂白性,物质F焰色反应呈黄色,则C的电子式为________;D中所含化学键的类型为________。
(2)若A为淡黄色固体,D为白色难溶于水的物质,且A和D的式量相等,请用离子方程式表示F的水溶液呈酸性的原因:_______________________。
(3)若A中一种元素原子的最外层电子数为内层电子总数的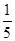 ,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:_____________________________________;
,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:_____________________________________;
B转化为C的化学方程式为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下列框图中的物质均为中学化学中常见物质,其中甲、乙为单质,其余均为化合物。B为常见液态化合物,A为淡黄色固体,将G的饱和溶液滴入沸水中,煮沸可得到红褐色胶体。请回答下列问题:
(1)A的电子式为 ,乙的组成元素在周期表中的位置是
(2)反应①~⑤中,属于非氧化还原反应的是 (填序号);C中含有的化学键有 (填序号:a离子键; b极性键 ;c 非极性键)
(3)反应⑤的化学方程式为 ;甲与B反应的离子方程式为 。
(4)F溶液中阳离子的检验方法为
(5)在F溶液中加入与F等物质的量的A恰好使F转化为E,写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
KHSO4、BaCl2、Na2CO3、FeSO4和氯水五种溶液,如图所示的相互反应,图中每条连线两端的物质可以发生化学反应。下列说法不合理的是( )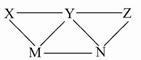
| A.X一定为KHSO4 | B.Y一定为Na2CO3 |
| C.Z可能是氯水 | D.M、N必定各为BaCl2、FeSO4中的一种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com