
(Ⅰ)地壳中含量第一金属元素构成的单质A与化合物B(相对分子质量为232)发生置换反应,产物为黑色固体C和另一单质D,单质D与水蒸气在高温下可得到B。则
(1)写出构成金属单质A的元素在周期表中的位置为 。
(2)写出D与水蒸气反应的化学方程式 。
(Ⅱ)某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用工艺设计如下:
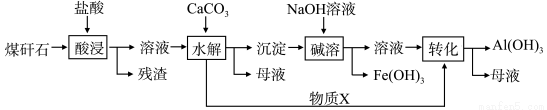
(3)物质X的化学式为___________。“碱溶”时反应的离子方程式为_____________。
(4)为加快“酸浸”时的速率,可采取的措施有 、 等。(填两种即可)
(5)已知Fe3+开始沉淀和沉淀完全的pH分别为2.1和3.2,Al3+开始沉淀和沉淀完全的pH分别为4.1和5.4。为了获得更多产品Al(OH)3,从煤矸石的盐酸浸取液开始,若只用CaCO3一种试剂,后续操作的实验方案是____________________________。
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源:2015-2016学年山东省淄博市高二上学期期中测试化学试卷(解析版) 题型:选择题
下列有关化学反应速率的说法中,正确的是
A.100 mL 2 mol/L的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变
B.用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率
C.二氧化硫的催化氧化是一个放热反应,升高温度,平衡逆向移动,正反应速率减慢
D.汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,加入催化剂,不影响CO的转化率
查看答案和解析>>
科目:高中化学 来源:2016届湖北省枣阳市高三上学期10月月考理综化学试卷(解析版) 题型:选择题
下列说法错误的是
A.第ⅤA族元素的几种气态氢化物中,NH3是稳定性最高的氢化物
B.由于C22—和O22+为等电子体,所以可以判断O22+的电子式为
C.含离子键的纯净物一定存在金属元素
D.某反应X(g)+Y(g)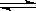 Z(g) △H<0 分两步进行:X(g)+Y(g)
Z(g) △H<0 分两步进行:X(g)+Y(g)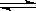 W(g) △H>0和W(g)
W(g) △H>0和W(g)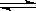 Z(g) △H<0,反应过程中的能量变化如右图:
Z(g) △H<0,反应过程中的能量变化如右图:

查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二上一次月考化学试卷(解析版) 题型:填空题
今有①盐酸、②醋酸、③硫酸三种稀溶液,用序号回答下列问题。
(1)若三种酸的物质的量浓度相等。
a.三种溶液中的c(H+)大小关系为__________________。
b.取等体积上述三种溶液,分别用同浓度的NaOH溶液完全中和,所需NaOH体积大小关系为 。
c.若取等质量Zn分别跟这三种溶液反应,使Zn恰好完全反应时,消耗三种酸的体积大小关系为 。
(2)若三种酸溶液中的c(H+)相等。
a.三种酸的物质的量浓度大小关系为__________________。
b.取等体积上述三种溶液,分别用同浓度的NaOH溶液完全中和,所需NaOH溶液体积大小关系为 。
C.取等质量Zn分别跟这三种溶液反应,使Zn恰好完全反应时,消耗三种酸的体积大小关系为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江哈尔滨六中高一10月月考化学试卷(解析版) 题型:选择题
在NaCl、MgCl2、MgSO4形成的混合溶液中,c(Na+)=0.1 mol/L,c(Mg2+)=0.25 mol/L,c(Cl-)=0.2 mol/L,则c(SO42-)为
A.0.15 mol/L B.0.10 mol/L
C.0.25 mol/L D.0.20 mol/L
查看答案和解析>>
科目:高中化学 来源:2016届江西省高安市高三上学期第二次段考化学试卷(解析版) 题型:选择题
中国历史悠久,很早就把化学技术应用到生产生活中。下列与化学有关的说法不正确的是
A.闻名世界的中国陶瓷、酿酒、造纸技术都充分应用了化学工艺
B.四大发明之一黑火药是由硫黄、硝石、木炭三种物质按一定比例混合制成
C.侯氏制碱法的工艺过程中应用了物质溶解度的差异
D.由于中国大部分地区都缺碘,而缺碘就会引起碘缺乏病,80年代国家强制给食用的氯化钠食盐中加入碘单质
查看答案和解析>>
科目:高中化学 来源:2016届山东省临沂市高三上学期10月阶段性教学质检化学试卷(解析版) 题型:选择题
下列有关氯元素及其化合物的表示正确的是
A.质子数为17、中子数为20的氯原子: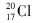
B.氯离子(Cl-)的结构示意图: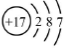
C.次氯酸分子的电子式: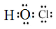
D.氯乙烯分子的结构简式:H3C-CH2Cl
查看答案和解析>>
科目:高中化学 来源:2016届四川省德阳市高三上学期10月月考理综化学试卷(解析版) 题型:简答题
氨气是一种重要工业原料,在工农业生产中具有重要的应用。
(1)已知:N2(g)+O2(g)=2NO(g) △ H=+180.5kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-905 kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1
则N2(g)+3H2(g)=2NH3(g)的△H=________________。
(2)工业合成氨气的反应为N2(g)+3H2(g) 2NH3(g)。在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是____________。
①增大压强 ②增大反应物的浓度 ③使用催化剂 ④降低温度
( 3 )①实验室常用加热氯化铵固体和氢氧化钙固体的混合物来制取氨气,画出反应及收集的简易装置;
实验室还可在 (填一种试剂)中滴加浓氨水的方法快速制取少量氨气。
② 常温下氨气极易溶于水,溶液可以导电。氨水中水电离出的c(OH-) 10-7 mol·L-1(填写“>”、“<”或“=”);
③ 将相同体积、PH之和为14的氨水和盐酸混合后,溶液中离子浓度由大到小的顺序为 。
(4)合成氨的原料氢气是一种新型的绿色能源,具有广阔的发展前景。现用氢氧燃料电池进行图所示实验:(其中a、b均为碳棒)。如右图所示:
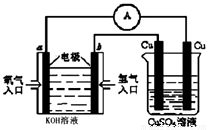
右边Cu电极反应式是 ,a电极的电极反应式
查看答案和解析>>
科目:高中化学 来源:2016届浙江省新安江校区高三上学期第二次模拟化学试卷(解析版) 题型:填空题
(12分)湿法炼锌的冶炼过程可用如图简略表示:

请回答下列问题:
(1)NH3的空间构型是 .氨气易液化,液氨常做制冷剂,氨气易液化的原因是_____________________.
(2)已知ZnO属于两性氧化物,写出ZnO与NaOH溶液反应的化学方程式: .
(3)上述电解过程中析出锌的电极反应式为 .
(4)产生的SO2可用Ba(NO3)2溶液吸收,部分产物可作为工业原料,其反应的离子方程式为
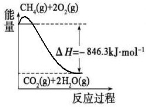
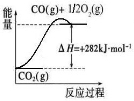
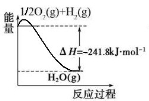
(5)氨是最重要的化工产品之一。合成氨用的氢气可以甲烷为原料制得:
CH4(g)+H2O(g) CO(g)+3H2(g)。有关化学反应的能量变化如下图所示,则CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为_______________________.
CO(g)+3H2(g)。有关化学反应的能量变化如下图所示,则CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为_______________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com