
氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)下列生产、生活中的事例中发生了氧化还原反应的是( )

(2)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用如图表达。

试写出有水参加、水为还原剂且为类型Ⅳ的一个化学方程式:_ _
(3)NaNO2是一种食品添加剂,它能致癌。酸性KMnO4溶液与NaNO2的反应离子方程式是
MnO4-+
NO2-+  =====
Mn2++ NO3-+ H2O
=====
Mn2++ NO3-+ H2O
Ⅰ、请补充完整,配平方程式并标出电子转移方向和数目
Ⅱ、某同学称取了7.9 g KMnO4固体,欲配制100 mL溶液。回答下列问题:
该实验中,使用容量瓶时要检查是否漏水,其操作是: 。
Ⅲ、不规范的实验操作会导致实验结果的误差。分析下列操作对实验结果的影响偏小 (请填序号):
①在溶解过程中有少量液体溅出烧杯外
②定容时仰视仪器上的刻度线
③定容后,将容量瓶振荡摇匀后,静置发现液面低于刻度线,于是又加入少量水至刻度线
IV、最后所得的溶液应存放在试剂瓶中,并贴上标签,请你填写该标签(如图)。

V、某同学用上述配好的KMnO4溶液滴定末知浓度的NaNO2溶液:
取20mL末知浓度的NaNO2溶液于锥形瓶;
取上述配好的KMnO4溶液于 (“酸式”或“碱式”)滴定管
滴定完成后消耗KMnO4溶液10mL则NaNO2溶液的浓度为
|
(1) ( D ) (2)F2+2H2O==4HF+O2
(3)Ⅰ、 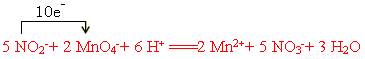
Ⅱ、往容量瓶中加入少量的蒸馏水,盖上瓶塞,倒置,看瓶塞是否漏水,放正,瓶塞旋转
180度,重新倒置,看是否漏水。
Ⅲ 、 ①②③ IV、 0.5mol/L KMnO4 V、酸式,0.625 mol/L
【解析】(1)凡是有元素化合价升降的反应都是氧化还原反应,燃烧是氧化还原反应,D正确,ABC都是物理变化,答案选D。
(2)类型Ⅳ是置换反应,所以满足有水参加、水为还原剂反应是F2+2H2O==4HF+O2。
(3)Ⅰ、根据方程式可知,锰元素的化合价从+7价降低到+2价,得到5个电子。氮元素的化合价从+3价升高到+5价,失去2个电子,所以根据电子的得失守恒可知,配平后的方程式是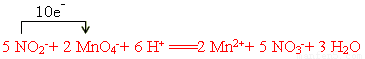 。
。
Ⅱ、检查容量瓶是否漏水的方法是往容量瓶中加入少量的蒸馏水,盖上瓶塞,倒置,看瓶塞
是否漏水,放正,瓶塞旋转180度,重新倒置,看是否漏水。
Ⅲ、根据c=n/V可知,在溶解过程中有少量液体溅出烧杯外,则溶质减少,浓度偏小;定容时仰视仪器上的刻度线,则容量瓶中溶液的体积增加,浓度偏小;又加入少量水至刻度线,则溶液体积增加,浓度偏小,答案选①②③。
IV、标签上面是溶液的浓度,下面是溶质的化学式。7.9 g KMnO4固体是0.05mol,所以浓
度是0.5mol/L。
V、高锰酸钾溶液碱液氧化性,能腐蚀橡胶,应该用酸式滴定管。根据方程式可知,亚硝酸钠的浓度是 =0.625 mol/L。
=0.625 mol/L。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com