
| A. | 13C和14C属于同一种元素,它们互为同位素 | |
| B. | 6Li和7Li的电子数相等,中子数也相等 | |
| C. | 14C和14N的质量数相等,它们的中子数不等 | |
| D. | 1H和2H是不同的核素,它们的质子数相等 |
分析 A.质子数相同,中子数不同的原子互为同位素;
B.原子中,质子数=电子数,质量数=质子数+中子数;
C.元素符号左上角的数字为质量数,质量数=质子数+中子数;
D.同位素的质子数相同.
解答 解:A.13C和14C的质子数相同,则属于同一种元素,但中子数不同,所以它们互为同位素,故A正确;
B.6Li和7Li的电子数相等,均为3,中子数分别为3、4,故B错误;
C.14C和14N的质量数相等,均为14,但它们的中子数分别为8、7,故C正确;
D.1H和2H是不同的核素,它们的质子数相等,均为1,故D正确;
故选B.
点评 本题考查原子的构成及原子中的数量关系,把握同位素的判断及原子中质子数=电子数、质量数=质子数+中子数为解答的关键,注重基础知识的考查,题目较简单.


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:解答题
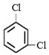
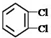 ;③35Cl、37Cl;
;③35Cl、37Cl;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+ | B. | Cu2+ | C. | Al3+ | D. | Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 第VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种价态,含第VIA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
第VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种价态,含第VIA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②③⑤ | B. | 只有③⑤⑥ | C. | 只有①③⑤ | D. | 只有①②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有第ⅠA族的元素所形成的单质在O2中燃烧时均可生成R2O(R代表碱金属元素) | |
| B. | 根据Mg(OH)2、Ca(OH)2、Ba(OH)2的溶解性,可推出Sr(OH)2可能在水中有较大的溶解度 | |
| C. | 第ⅥA族元素形成的化合物种类最多 | |
| D. | 若用NA表示阿伏伽德罗常数,则4.4g CO2中含有电子的数目为0.8NA个e- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚溶液、乙烷、乙烯、乙醇、溴苯4种物质可用溴水一次鉴别 | |
| B. | CH3CH2OH、CH2=CHCOOH、CH3CHO、CH3COOH四种溶液可用新制Cu(OH)2一次鉴别 | |
| C. | 除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤 | |
| D. | KCl溶液中混有少量KI,可通入足量Cl2后,再用乙醇进行萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
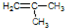 ,其系统命名为2-甲基-1-丙烯.
,其系统命名为2-甲基-1-丙烯.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com