
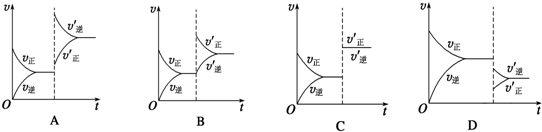
分析 (1)催化剂能同等程度的改变正逆反应速率,但该反应仍然呈平衡状态,平衡不移动;
(2)升高温度,增大正逆反应速率,逆反应速率增大程度大于正反应速率,平衡逆向移动;
(3)增大氧气浓度,正反应速率增大,改变条件瞬间,逆反应速率不变,随着反应的进行,平衡正向移动.
解答 解:(1)加入催化剂,正、逆反应速率均增大,图象上应该出现“断点”,且应在原平衡的反应速率之上;催化剂使正、逆反应速率增大的倍数相同,则改变条件后的速率线应该平行于横坐标轴,图象为C,
故答案为:C;
(2)升高温度,正、逆反应速率均增大,图象上应该出现“断点”且应在原平衡的反应速率之上,因题给反应的正反应放热,升温平衡逆向移动,所以v正′<v逆′,图象为A,
故答案为:B;逆反应;
(3)增大O2的浓度,正反应速率会“突然增大”,图象上出现“断点”且应在原平衡的反应速率之上,但逆反应速率应该在原来的基础上逐渐增大,图象为B,故答案为:B.
点评 本题考查v-t图象分析,为高频考点,侧重考查学生分析判断能力,明确外界条件对反应速率、平衡影响原理是解本题关键,会根据图象中v变化特点及正逆反应速率相对大小判断可能改变的条件,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150 mL 1 mol•L-1的NaCl溶液 | B. | 75 mL 2 mol•L-1NH4Cl溶液 | ||
| C. | 150 mL 2 mol•L-1的KCl溶液 | D. | 100 mL 1.5 mol•L-1FeCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
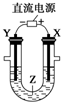
| A. | 氯碱工业中,X电极上反应式是4OH--4e-═2H2O+O2↑ | |
| B. | 电解精炼铜时,Z溶液中的Cu2+浓度不变 | |
| C. | 在铁片上镀铜时,Y是纯铜 | |
| D. | 制取金属镁时,Z是熔融的氯化镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中溶液变浑浊,可能有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有Ag+ | |
| C. | 加入氢氧化钠溶液并加热,产生的气体能使湿润蓝色石蕊试纸变红,一定有NH4+ | |
| D. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ca2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 图为某市售浓盐酸试剂瓶标签上的部分数据.
图为某市售浓盐酸试剂瓶标签上的部分数据.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三种 | B. | 四种 | C. | 五种 | D. | 六种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com