
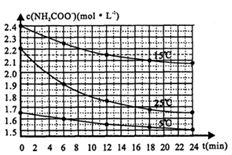
 某研究小组在实验室用三份不同初始浓度的氨基甲酸铵(NH2COONH4)溶液在不同温度下进行水解实验:NH2COONH4+2H2O?NH4CO3+NH3?H2O,测得c(NH2COO-)与反应时间的关系如图所示.据图判断下列说法正确的是( )
某研究小组在实验室用三份不同初始浓度的氨基甲酸铵(NH2COONH4)溶液在不同温度下进行水解实验:NH2COONH4+2H2O?NH4CO3+NH3?H2O,测得c(NH2COO-)与反应时间的关系如图所示.据图判断下列说法正确的是( )| 1.65mol/L-1,55mol/L |
| 12min |
| 2.2mol/L-1.75mol/L |
| 12min |
| 2.4mol/L-2.15mol/L |
| 12min |
| 2.2mol/L-1.9mol/L |
| 6min |
| 1.65mol/L-1,55mol/L |
| 12min |
| 2.2mol/L-1.75mol/L |
| 12min |
| 2.4mol/L-2.15mol/L |
| 12min |
| 2.2mol/L-1.9mol/L |
| 6min |


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
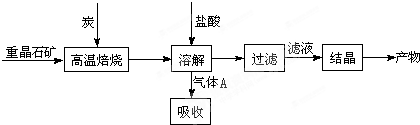
| 高温 |
| 高温 |
| c(Br-) |
| c(Cr-) |
| 高温 |
查看答案和解析>>
科目:高中化学 来源: 题型:
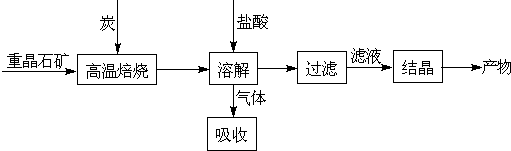
| ||
| ||
| c(Br-) |
| c(Cl-) |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
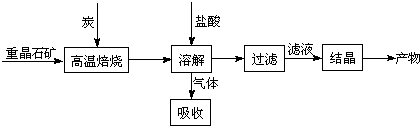
| 高温 |
| 高温 |
| 高温 |
| 光合作用 |
| 催化剂 |
| △ |
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
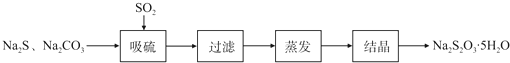
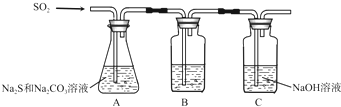
| 序号 | 实验操作 | 预期现象 | 结论 |
| ① | 取少量样品于试管中,加入适量蒸馏水,充分振荡溶解, |
样品含NaCl | |
| ② | 另取少量样品于烧杯中,加入适量蒸馏水,充分搅拌溶解, |
样品含NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com