
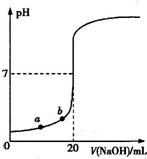
 用0.100 0mol?L-1 NaOH溶液滴定20.00mL未知浓度的盐酸(酚酞作指示剂)的滴定曲线如图所示.下列说法正确的是( )
用0.100 0mol?L-1 NaOH溶液滴定20.00mL未知浓度的盐酸(酚酞作指示剂)的滴定曲线如图所示.下列说法正确的是( )| 0.02L×0.1mol/L-0.01L×0.1mol/L |
| 0.03L |
| 0.02L×0.1mol/L-0.01L×0.1mol/L |
| 0.03L |
| 1 |
| 3 |


科目:高中化学 来源: 题型:阅读理解
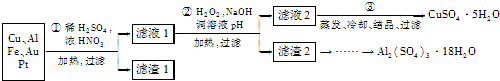
| 沉淀物 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
| 开始沉淀 | 5.8 | 1.1 | 4.0 | 5.4 |
| 完全沉淀 | 8.8 | 3.2 | 5.2 | 6.7 |
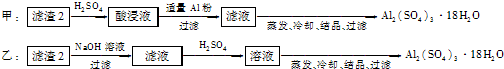
2- 3 |
2- 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液呈中性,可选用甲基橙或酚酞作指示剂 | B、溶液呈中性,只能选用石蕊作指示剂 | C、溶液呈酸性,可选用甲基橙作指示剂 | D、溶液呈碱性,只能选用酚酞作指示剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
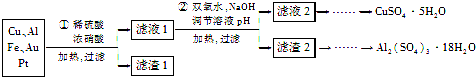
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,用0.100 0mol·L-1 NaOH溶液滴定20.00 mL 0.100 00 mol·L-1 CH3COOH溶液滴定曲线如图所示。下列说法正确的是
A.点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
B.点②所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-)
C.点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com