
A.x=10时,溶液中有 、Al3+、 、Al3+、 ,且c( ,且c( )>c(Al3+) )>c(Al3+) |
B.x=10时,溶液中有 、 、 、 、 ,且c( ,且c( )>c( )>c( ) ) |
C.x=30时,溶液中有Ba2+、 、OH﹣,且c(OH﹣)<c( 、OH﹣,且c(OH﹣)<c( ) ) |
| D.x=30时,溶液中有Ba2+、Al3+、OH﹣,且c(OH﹣)=c(Ba2+) |


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源:不详 题型:单选题
| A.x=2 | B.氧化产物和还原产物的比为2:5 |
| C.生成4mol H2O转移10mol电子 | D.MOyx-中的M的化合价为+7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++ SO42- =BaS04↓+2H2O |
| B.酸性介质中KMnO4氧化 H2O2:2MnO4-+5H2O2+6H+ = 2Mn2++5O2↑+ 8H2O |
| C.等物质的量的MgCl2、Ba(OH)2和 HC1 溶液混合:Mg2++2OH-= Mg(OH)2↓ |
| D.铅酸蓄电池充电时的正极反应:PbSO4+ 2H2O-2e- = PbO2+4H++SO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe(OH)2溶液中加入HNO3溶液:Fe(OH)2+2H+=2H2O+Fe2+ |
| B.盐酸除去铜器表面的铜绿:Cu2(OH)2CO3+4H+=3H2O+2Cu2++CO2↑ |
| C.氯气可以降低的SO2的漂白性:SO2+Cl2+2H2O=2Cl—+4H++SO42— |
| D.CO2通入饱和碳酸钠溶液:CO2+ CO32—+2Na++H2O=2NaHCO3↓ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③⑥⑨ | B.②④⑤⑨ | C.③④⑦⑧ | D.①⑧⑨ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 时,亚磷酸(
时,亚磷酸( ,二元酸)的
,二元酸)的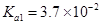 ,
, ;
; )的
)的 ,
,
| A.Mg2++2HCO3-+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O |
B. |
C. |
D. |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
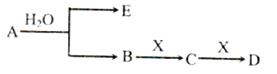
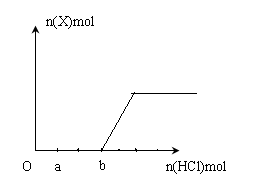
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向AgCl悬浊液中加入Na2S溶液:2AgCl +S2- ="=" Ag2S+ 2Cl- |
| B.向NaHCO3溶液中加入NaOH溶液: HCO3-+OH- == + H2O |
| C.向Ba(OH)2溶液中加入稀H2SO4:Ba2+ + OH-+ H+ + ="=" BaSO4↓+ H2O |
| D.向Cu粉中加入过量的浓HNO3:Cu+4H+ +2="=" Cu2++2NO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com