
科目:高中化学 来源: 题型:
(1)甲醇是一种优质燃料,可制作燃料电池。
①工业上可用下列两种反应制备甲醇:
 CO(g) + 2H2(g)
CO(g) + 2H2(g)  CH3OH(g) ΔH1
CH3OH(g) ΔH1
CO2(g)+3H2(g)  CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
已知:2H2(g)+ O2(g) = 2H2O(g) ΔH3
则2CO(g)+O2(g) =2CO2(g) 的反应热ΔH=_____________(用ΔH1、ΔH2、ΔH3表示)。
②生产甲醇的原料CO和H2来源于:CH4(g) + H2O(g)  CO(g) + 3H2(g) ΔH4。
CO(g) + 3H2(g) ΔH4。
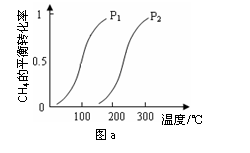
一定条件下CH4的平衡转化率与温度、压强的关系如图a。则ΔH4______0,P1_________P2
(填“<”、“>”或“=”);
(2)用CO2来生产燃料甲醇的反应原理:CO2(g)+3H2(g)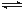 CH3OH(g)+H2O(g),某些化学键的键能数据如下表:
CH3OH(g)+H2O(g),某些化学键的键能数据如下表:
| 化学键 | C-C | C-H | H-H | C-O | C=O | H-O |
| 键能/kJ·mol-1 | 348 | 413 | 436 | 358 | 750 | 463 |
计算反应上述反应的焓变△H=_____________。
(3)氢气燃烧生成液态水的热化学方程式是2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ/mol
请回答下列问题:
①生成物能量总和 (填“大于”、“小于”或“等于”)反应物能量总和
②若2 mol氢气完全燃烧生成水蒸气,则放出的热量 572 kJ(填“大于”、“小于”或“等于”)
(4)已知:
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) ΔH1=—890.3 kJ/mol
2CO (g) + O2(g) = 2CO2(g) ΔH2=—566.0 kJ/mol
则甲烷不完全燃烧生成一氧化碳和液态水时的热效率是完全燃烧时的________倍(计算结果保留1位小数)。
(5)已知热化学方程式如下:N2(g)+3H2O(1)==2NH3(g)+ O2(g);△H=+765.2 kJ·mol-1,请在答题卡的坐标图中,画出上述反应过程中体系能量变化示意图,并进行必要标注。
O2(g);△H=+765.2 kJ·mol-1,请在答题卡的坐标图中,画出上述反应过程中体系能量变化示意图,并进行必要标注。
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生的实验报告所列出的下列数据中合理的是
A.用10mL量筒量取7.13mL稀盐酸 B.用托盘天平称量25.20g NaCl
C.用广范pH试纸测得某溶液的pH为2.3
D.用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70mL
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)今有2H2+O2 2H2O反应,构成燃料电池,则电极反应式为:负极____________________、正极__________________。
2H2O反应,构成燃料电池,则电极反应式为:负极____________________、正极__________________。
(2)如把H2改为甲烷,KOH做导电物质,则负极电极反应式为_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
根据氢原子和氯原子的核外电子排布,对Cl2和HCl分子中形成的共价键描述正确的
A.两者都为s s σ键
s σ键
B.两者都为p p σ键
p σ键
C.前者为p p σ键,后者为s
p σ键,后者为s p σ键
p σ键
D.前者为s s σ键,后者为s
s σ键,后者为s p σ键
p σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
氰气的化学式为(CN)2,结构式为N≡C—C≡N,性质与卤素相似,下列叙述正确的是
A.在一定条件下可发生加成反应
B.分子中N≡C键的键长大于C—C键的键长
C.分子中含有2个σ键和4个π键
D.不和氢氧化钠溶液发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
SF6是一种优良的绝缘气体,分子结构中只存在S-F键。已知:1molS(s)转化为气态硫原子吸收能量280kJ,断裂1molF-F 、S-F键需吸收的能量分别为160kJ、330kJ。
则S(s)+3F2(g)=SF6(g)的反应热△H为
A.-1780kJ/mol B.-1220 kJ/mol C.-450 kJ/mol D.+430 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下设a代表Ba(OH)2,b代表NaOH溶液,c代表NH3·H2O溶液。下列说法正确的是
A.同物质的量浓度的三种溶液的pH:a>b>c
B.同pH时,三种溶液稀释相同倍数后的pH:a<b<c
C.同pH、同体积的三种溶液消耗同浓度盐酸的体积:a=b=c
D.同pH时,稀释不同倍数后pH仍相同,三种溶液稀释的倍数:a>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用于判断元素金属性强弱的是( )
A.1 mol金属单质在反应中失去电子的多少
B.金属单质之间发生的置换反应
C.金属元素最高价氧化物对应的水化物的碱性强弱
D.金属元素的单质与水或酸置换出氢气的难易程度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com