C
分析:A、PH计算氢离子浓度,依据n=cV计算溶质物质的量;
B、依据n=
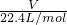
计算标准状况下气体物质的量,结合氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,氯元素化合价从0价变化为+1价和-1价;
C、乙烯和丁烯最简式相同为CH
2,依据n=

计算21.0 gCH
2中的碳原子数;
D、铁离子水解;
解答:A、pH=1的溶液中c(H
+)=0.1mol/L,1.0 L H
2SO
4溶液中含有的H
+的数目为0.1N
A,故A错误;
B、标准状况下,2.24 L Cl
2物质的量0.1mol,与过量稀NaOH溶液反应,氯元素化合价从0价变化为+1价和-1价;电子转移数为0.1N
A,故B错误;
C、乙烯和丁烯最简式相同为CH
2,计算21.0 gCH
2中的碳原子数=
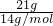
×N
A=1.5N
A,故C正确;
D、取0.5 L 0.2 mol?L
-1mol氯化铁溶液,铁离子水解,所得溶液含铁离子小于0.1 N
A个Fe
3+,故D错误;
故选C.
点评:本题考查了阿伏伽德罗常数的应用,主要考查溶液浓度计算,气体摩尔体积的条件应用,盐类水解的分析,题目难度中等.

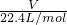 计算标准状况下气体物质的量,结合氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,氯元素化合价从0价变化为+1价和-1价;
计算标准状况下气体物质的量,结合氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,氯元素化合价从0价变化为+1价和-1价; 计算21.0 gCH2中的碳原子数;
计算21.0 gCH2中的碳原子数;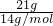 ×NA=1.5NA,故C正确;
×NA=1.5NA,故C正确;

 阅读快车系列答案
阅读快车系列答案