

| A. | 气体W为氧气 | |
| B. | b极与电源的正极相连 | |
| C. | 离子交换膜c为阳离子交换膜 | |
| D. | a极的电极反应为SO2+2H2O-2e-=SO42-+4H+. |
分析 根据图知,右边装置中加入较稀的NaOH溶液,电解后得到较浓的NaOH溶液,说明b电极上发生的反应为2H2O-4e-=2H2↑+4OH-,所以b是阴极、a是阳极,左边装置中,加入稀硫酸和SO2,电解后得到较浓的硫酸,电极反应式为SO2+2H2O-2e-=SO42-+4H+.
解答 解:根据图知,右边装置中加入较稀的NaOH溶液,电解后得到较浓的NaOH溶液,说明b电极上发生的反应为2H2O-4e-=2H2↑+4OH-,所以b是阴极、a是阳极,左边装置中,加入稀硫酸和SO2,电解后得到较浓的硫酸,电极反应式为SO2+2H2O-2e-=SO42-+4H+;
A.通过以上分析知,b电极上得到的气体是H2,即w是H2,故A错误;
B.b是阴极,连接电源负极,故B错误;
C.a电极上生成氢离子,需要硫酸根离子形成硫酸,所以离子交换膜c阴离子交换膜,故C错误;
D.左边装置中,加入稀硫酸和SO2,电解后得到较浓的硫酸,电极反应式为SO2+2H2O-2e-=SO42-+4H+,故D正确;
故选D.
点评 本题考查电解原理,为高频考点,侧重考查学生观察、分析判断、知识运用能力,明确各个电极上发生的反应、电极名称的判断是解本题关键,题目难度不大.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 若容器内压强不再变化,则说明该反应己达平衡 | |
| B. | 反应前H2S物质的量为2.5mol | |
| C. | CO和H2S达平衡后的转化率相同 | |
| D. | 若平衡后再加入CO,则正反应速率增大,逆反应速率减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高体系温度,平衡常数K减小 | |
| B. | 增大体系压强,平衡常数K不发生变化 | |
| C. | 平衡常数表达式为K=$\frac{[CO][{H}_{2}]}{[C][{H}_{2}O]}$ | |
| D. | 增加C(s)的量,平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
| A. | 上述生成Ni(CO)4的反应为放热反应 | |
| B. | 在80℃时,测得某时刻Ni(CO)4、CO的浓度均为0.5 mol•L-1,则此时v正>v逆 | |
| C. | 25℃时反应Ni(CO)4(g) Ni(s)+4CO(g)的平衡常数为2×10-5 | |
| D. | 80℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②③ | B. | 只有③④ | C. | 只有①③ | D. | 只有①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
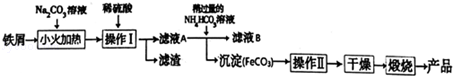
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧燃料电池是一种将化学能转化为电能的装置 | |
| B. | 铁船舶的外壳上镶嵌锌块,可避免船体遭受腐蚀 | |
| C. | 钢铁腐蚀时负极的电极反应式:Fe-3e-═Fe+ | |
| D. | 工业上电解饱和食盐水时阴极的电极反应式:2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
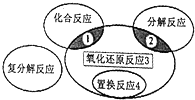 氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是( )
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是( )| A. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | B. | 2Na2HCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O | ||
| C. | 2Na2O2+2H2O═4NaOH+O2↑ | D. | Zn+H2SO4═ZnSO4+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com