
| A��������ʴʱ���ܷ�����������Ӧ��2H2O + O2 + 4e��= 4OH�� |
| B����KHSO4��Һ�е���Ba(OH)2��ҺʹpH=7��SO42��+ 2 H+ + Ba2+ + 2OH��= BaSO4��+ 2 H2O |
C������ˮ������ӷ���ʽ��Al3+ + 3H2O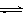 Al(OH)3 + 3H+ Al(OH)3 + 3H+ |
| D��K37ClO3��Ũ����(HCl)�ڼ���ʱ����������K37ClO3 + 6HCl��K37Cl + 3Cl2��+ 3H2O |
 2KCl+37Cl2��+5Cl2��+6H2O����D����
2KCl+37Cl2��+5Cl2��+6H2O����D����

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Ca2+��HCO3-��K+��NO3- | B��HCO3-��H+��Ba2+��Na+ |
| C��HCO3-��OH-��Al3+��Na+ | D��Mg2+��Fe3+��OH-��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���Ȼ�����Һ�м��������ˮ��Al3����4NH3��H2O=AlO2����4NH4+��2H2O |
| B��Ũ�ռ���Һ�м�����Ƭ��Al��2OH��=AlO2����H2�� |
| C����ŨNaOH��Һ�ܽ�Al2O3��2OH����Al2O3=2AlO2����H2O |
| D����̼��þ�еμ�ϡ���CO32����2H��=CO2����H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NH4+ NO3- CO32- Na�� |
| B��Na��Ba2��Mg2��HCO3- |
| C��NO3- K��AlO2- OH�� |
| D��NO3- Ca2��K��Cl�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ʹ���ȱ��ɫ����Һ��Mg2����K����SO42����NO3�� |
B��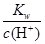 ��0.1 mol��L��1����Һ��Na����Cu2����HCO3����NO3�� ��0.1 mol��L��1����Һ��Na����Cu2����HCO3����NO3�� |
| C��������CH4��CO2��SO2��NO |
| D��0.1 mol��L��1 NaAlO2��Һ��H����Na����Cl����SO42�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���п��Ľ���Na��¶�ڿ����У����������䰵2Na��O2=Na2O2 |
| B����AgCl����Һ�еμ�Na2S��Һ����ɫ������ɺ�ɫ2AgCl��S2��=Ag2S����2Cl�� |
| C��Na2O2�ڳ�ʪ�Ŀ����з���һ��ʱ�䣬��ɰ�ɫճ����2Na2O2��2CO2=2Na2CO3��O2 |
| D����NaHCO3��Һ�м�������ij���ʯ��ˮ�����ְ�ɫ����2HCO3-��Ca2����2OH��=CaCO3����CO32-��2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A����ʹpH��ֽ����ɫ����Һ�У� |
B��������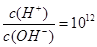 ����Һ�У� ����Һ�У� 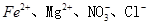 |
C�����д���Al3+����Һ�У�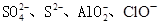 |
| D��������pHΪ7����Һ�У� K+��Fe3�� ��Cl-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 NH3�� + H2O��NH3��ʹʪ��ĺ�ɫʯ����ֽ��������ij��Һ�п��ܺ�������6�������е�ij���֣�Na+��NH4+��K+��Cl����SO42����CO32����Ϊȷ����Һ��ɽ�������ʵ�飺��1��ȡ200 mL������Һ����������BaCl2��Һ����Ӧ�������ˡ�ϴ�ӡ�����ó���4.30g��������м�����������ᣬ��2.33g�������ܡ���2����1������Һ�м���������NaOH��Һ�����ȣ�������ʹʪ���ɫʯ����ֽ����������1.12L���ѻ���ɱ�״�����ٶ�����������ȫ���ݳ������ɴ˿��Եó�����ԭ��Һ��ɵ���ȷ������
NH3�� + H2O��NH3��ʹʪ��ĺ�ɫʯ����ֽ��������ij��Һ�п��ܺ�������6�������е�ij���֣�Na+��NH4+��K+��Cl����SO42����CO32����Ϊȷ����Һ��ɽ�������ʵ�飺��1��ȡ200 mL������Һ����������BaCl2��Һ����Ӧ�������ˡ�ϴ�ӡ�����ó���4.30g��������м�����������ᣬ��2.33g�������ܡ���2����1������Һ�м���������NaOH��Һ�����ȣ�������ʹʪ���ɫʯ����ֽ����������1.12L���ѻ���ɱ�״�����ٶ�����������ȫ���ݳ������ɴ˿��Եó�����ԭ��Һ��ɵ���ȷ������| A��һ������SO42����CO32����NH4+�����ܴ���Na+��K+��Cl�� |
| B��һ������SO42����CO32����NH4+��Cl����һ��������Na+��K+ |
| C��c(CO32��)="0.01" mol/L��c(NH4+)��c(SO42��) |
| D���������6�����Ӷ����ڣ���c(Cl��)��c(SO42��) |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com