
| A、HA水溶液中微粒浓度大小顺序:c(HA)>c(H+)>c(A-)>c(OH-) |
| B、HA与NH3作用生成的化合物是共价化合物 |
| C、NaA水溶液中:c(Na+)=c(A-)+c(HA) |
| D、稀释0.1mol/LHA水溶液,其电离程度增大,pH也增大 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、若向容器中充入1molN2和3molH2,最终生成2molNH3 |
| B、达到平衡时,体系中各物质的浓度不在改变 |
| C、使用催化剂是为了加快反应速率 |
| D、增大氮气的浓度可加快反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向10mL 0.2mol/L NaOH溶液中依次滴入2滴0.1mol/L MgCl2溶液,2滴0.1mol/L FeCl3溶液 | 先生成白色沉淀,后生成红褐色沉淀 | 相同温度下的Ksp:Mg(OH)2>Fe(OH)3 |
| B | 向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色沉淀 | 溶液X中一定含有 SO42- |
| C | 将蔗糖溶液与稀硫酸混合水浴加热,取反应后的溶液少量,加入几滴新制的Cu(OH)2悬浊液加热 | 未出现砖红色沉淀 | 蔗糖没有水解 |
| D | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 溶液红色变浅 | Na2CO3溶液中存在水解平衡 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、2.9g C2H
| ||
| B、标准状况下,22.4L乙酸的分子数为NA个 | ||
| C、一个氯原子的质量是35.5NAg | ||
| D、铝与氢氧化钠溶液反应,每生成1mol氢气,铝就失去2NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原电池是将电能转化为化学能的一种装置 |
| B、用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 mol NaOH |
| C、在原电池的负极和电解池的阴极上都发生失电子的氧化反应 |
| D、.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化铝溶液中加入过量氨水:Al3++4OH-→AlO2-+2H2O |
| B、碳酸钙与盐酸反应:CaCO3+2H+→Ca2++CO2↑+H2O |
| C、锌粉溶解于醋酸:Zn+2H+→Zn2++H2↑ |
| D、硫酸镁溶液跟氢氧化钡溶液反应:Mg2++SO42-+Ba2++2OH-→BaSO4↓+Mg(OH)2↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B |
 制备并收集氨气 |  验证铁的吸氧腐蚀 |
| C | D |
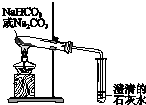 鉴别碳酸钠与碳酸氢钠 | 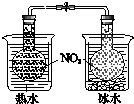 证明温度对平衡移动的影响 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com