
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
下列化学反应的离子方程式书写正确的是
A.氯气通入氯化亚铁溶液中:Fe2++Cl2== 2Cl-+Fe3+
B.氯气与水反应:Cl2 + H2O== Cl-+ ClO- + 2H+
C.铜与稀硝酸反应:3Cu + 8H+ + 2NO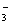 == 3Cu2+ + 2NO↑ + 4H2O
== 3Cu2+ + 2NO↑ + 4H2O
D.三氯化铝中加入过量的氨水:Al3++4 NH3·H2O = AlO2— +4 NH4+ + 2 H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验室中,对下列事故或药品的处理正确的是
A . 有大量的氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场
B. 金属钠着火燃烧时,用泡沫灭火器灭火
C. 少量浓硫酸沾在皮肤上,立即用大量的氢氧化钠溶液冲洗
D. 含硫酸的废液倒入水槽,用水冲入下水道
查看答案和解析>>
科目:高中化学 来源: 题型:
如图判断,下列说法正确的是 ]
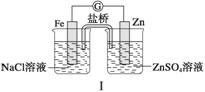
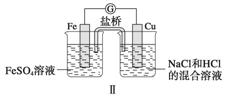
A.装置Ⅰ和装置Ⅱ中负极反应均是Fe-2e-===Fe2+
B.装置Ⅰ和装置Ⅱ中正极反应均是O2+2H2O+4e-===4OH-
C.装置Ⅰ和装置Ⅱ中盐桥中的阳离子均向右侧烧杯移动
D.放电过程中,装置Ⅰ左侧烧杯和装置Ⅱ右侧烧杯中溶液的pH均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
I、(8分)以下是依据一定的分类标准,对某些物质与水的反应情况进行分类的分类图。请根据你所学的知识按要求填空:
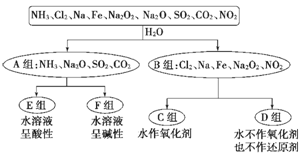
(1)上述第一级分类标准(分成A、B组的依据)是:__________________
(2)D组物质包括_________________________________(填化学式)。
(3)C组物质中某一物质在常温时能与冷水反应,其化学方程式为_________。
(4)D组中某一物质与E组中某一物质在水中反应生成两种强酸,写出该反应的离子方程式:_______________________________________________________。
II、(10分)下图中每一方格表示有关的一种反应物或生成物。A、C为无色气体。
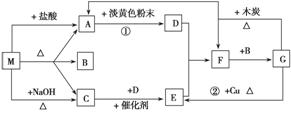
(1)、物质M可以是________或________,C是________,F是________。
(2)、反应①的化学方程式_________________________________________。
(3)、反应②的离子方程式_______________________________________________。
(4)、F→G的化学方程式___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
分类法是一种行之有效、简单易行的科学方法。某同学用如表所示的形式对所学知识进行分类,甲与乙、丙、丁是包含关系。其中正确的是
| 选项 | 甲 | 乙、丙、丁 |
| A | 弱电解质 | 一水合氨、水、硫酸钡 |
| B | 腐蚀品 | 浓硫酸、烧碱、硝酸 |
| C | 碱性氧化物 | 过氧化钠、氧化镁、氧化铁 |
| D | 合成高分子材料 | 光导纤维、涤纶、玻璃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是
A.金属单质与盐溶液的反应都是置换反应
B.4Fe(OH)2+O2+2H2O=4Fe(OH)3属于化合反应
C.SO2+Cl2+2H2O=2HCl+H2SO4属于氧化还原反应
D.AgNO3+HCl=AgCl↓+ HNO3该反应不能说明盐酸酸性比硝酸强
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如下。
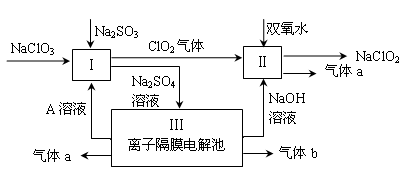 |
(1)Ⅰ中发生反应的还原剂是 (填化学式)。
(2)Ⅱ中反应的离子方程式是 。
(3)A的化学式是 ,气体b的化学式是 ,
装置Ⅲ中发生反应的化学方程式是 。
(4)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:
5NaClO2 + 4HCl = 5NaCl + 4ClO2↑ + 2H2O。
① 该反应中氧化剂和还原剂的物质的量之比是 。
② 研究表明:若反应开始时盐酸浓度越大,则气体产物中Cl2的含量越大,运用氧化还原反应规律分析其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
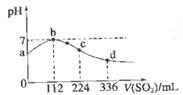 标准状况下,向100 mL H2S饱和溶液中通入SO2气体,
标准状况下,向100 mL H2S饱和溶液中通入SO2气体,
所得溶液pH变化如图中曲线所示。下列分析正确的是
A.原H2S溶液的物质的量浓度为0.05 mol/L
B.氢硫酸的酸性比亚硫酸的酸性强
C.b点水的电离程度比c点水的电离程度大
D.a点对应溶液的导电性比d点强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com