
����Ŀ���ۺ���H ( )��һ�־�������ά���㷺���ڸ���ɲ��Ƭ����ϳ�·�����£�
)��һ�־�������ά���㷺���ڸ���ɲ��Ƭ����ϳ�·�����£�

��֪����C��D��G��Ϊ�����廯��������о�ֻ�����ֲ�ͬ��ѧ��������ԭ�ӡ�
��Diels-Alder��Ӧ��![]() ��
��
��1������A�ķ�Ӧ������_______��D��������_______��F�����������ŵ�������_______��
��2��B�Ľṹ��ʽ��_______����B��C���ķ�Ӧ�У���C�⣬����һ�ֲ�����_______��
��3��D+G��H�Ļ�ѧ����ʽ��______��
��4��Q��D��ͬϵ���Է���������D��14����Q���ܵĽṹ��______�֣����к˴Ź���������4��壬�ҷ������Ϊ1:2:2:3�Ľṹ��ʽΪ______����дһ�֣���
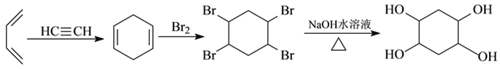
��5����֪����Ȳ��1,3-����ϩҲ�ܷ���Diels-Alder��Ӧ������1,3-����ϩ����ȲΪԭ�ϣ�ѡ�ñ�Ҫ�����Լ��ϳ� ��д���ϳ�·��__________���ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ��������
��д���ϳ�·��__________���ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ��������
���𰸡� ��ȥ��Ӧ �Ա������� ��������ԭ�� 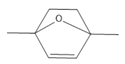 H2O n
H2O n![]() + n
+ n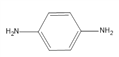
![]()
![]() + ��2n-1��H2O 10
+ ��2n-1��H2O 10 
���������������⣬A��![]() ��CΪ��
��C��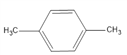 ,D��
,D��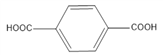 ��E��
��E��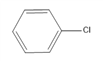 ��F��
��F��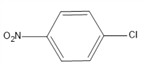 ��G��
��G��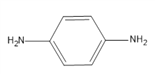 ��
��
��1�������Ҵ���������ˮ������ϩ��������A�ķ�Ӧ����Ϊ����ȥ��Ӧ��DΪ�� ������Ϊ���Ա������ᣬF��
������Ϊ���Ա������ᣬF�� �����������ŵ���������������ԭ�ӣ�
�����������ŵ���������������ԭ�ӣ�
��2��B����ϩ��![]() ���ɣ���B�Ľṹ��ʽ�ǣ�
���ɣ���B�Ľṹ��ʽ�ǣ� ����B��C���ķ�Ӧ��Ϊ��������ˮ����C�⣬����һ�ֲ�����ˮ��
����B��C���ķ�Ӧ��Ϊ��������ˮ����C�⣬����һ�ֲ�����ˮ��
��3��D�� ��G��
��GΪ�� ��HΪ
��HΪ![]() ����D+G��H�Ļ�ѧ����ʽ�ǣ�n
����D+G��H�Ļ�ѧ����ʽ�ǣ�n + n
+ n
![]()
![]() + ��2n-1��H2O��
+ ��2n-1��H2O��
��4��Q��D��ͬϵ���Է���������D��14�����һ��CH2�������г��˱��������������Ȼ���̼ԭ�ӻ�ʣ��1������������ֻ��һ��ȡ��������Ϊ-CH(COOH)2,��һ�֣���������ȡ��������Ϊ-COOH��-CH2COOH�������ڱ����ϵ�λ��Ϊ�ڼ�����֣���������ȡ��������Ϊ�����Ȼ���һ�������ȿ��ɱ������ᣬ�������������Ȼ���λ������Q���ܵĽṹ���ڼ�ԣ��������ϵ�H�ٱ���ȡ���ķֱ���2�֡�3��1�֣��ܼƹ�10��ͬ���칹�壻���к˴Ź���������4��壬�ҷ������Ϊ1:2:2:3�Ľṹ��ʽΪ ��
��
��5����Ȳ��1,3-����ϩҲ�ܷ���Diels-Alder��Ӧ��img src="http://thumb.zyjl.cn/Upload/2018/11/20/10/e7a4d9c2/SYS201811201003112366836299_DA/SYS201811201003112366836299_DA.015.png" width="165" height="79" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" />����1,3-����ϩ����ȲΪԭ�ϣ��ϳ�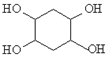 ���ϳ�˼·Ϊ�����÷�Ӧ
���ϳ�˼·Ϊ�����÷�Ӧ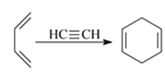 �ϳ���Ԫ��������±�ؼӳɣ�������������ˮ��Һȡ�����ɺϳɲ���ʺϳ�·��Ϊ��
�ϳ���Ԫ��������±�ؼӳɣ�������������ˮ��Һȡ�����ɺϳɲ���ʺϳ�·��Ϊ�� ��
��


 �������ͬ������ϵ�д�
�������ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������㶹����һ����������Ѫ�ܼ�����ҩ����谭Ѫ˨��չ�������㶹�ؿ���ͨ�����·����ϳɣ����ַ�Ӧ����ʡ�ԣ���

��֪��a��![]()
b����������Ϊһ���ӱ�������ȥ������ˮ��IJ�������ʽΪC3O2���÷���Ϊ��״�ṹ
�ش��������⣺
��1�������㶹���к��й����ŵ�������___________________��
��2��C�Ľṹ��ʽΪ��_____________��
��3��E��G���ɴ����㶹�صķ�Ӧ����Ϊ____________��
��4��д�����б����������������G�Ļ�ѧ����ʽ_______________________��
��5����Ӧ�۵Ļ�ѧ����ʽΪ_______________________________________��
��6������E���ʣ�����˵����ȷ����_______������ĸ��ţ���
a���ں˴Ź������������������շ�
b��������������Ӧ����D��E
c�����Է����ӳɷ�Ӧ�����۷�Ӧ��������Ӧ�ͻ�ԭ��Ӧ
d������˳���칹
��7�����ӽṹ��ֻ����һ��������ͬʱ��������������G��ͬ���칹�干��____�֡�
�ٿ����Ȼ�����Һ������ɫ��Ӧ���ڿ���̼��������Һ��Ӧ���ɶ�����̼���塣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��Ӧ�����ӷ���ʽ��ȷ����(����)
A. ��С�մ�����θ����ࣺHCO3-��H��===CO2����H2O
B. ��̼��þ�еμ�ϡ���CO32-��2H��===CO2����H2O
C. ������ʯ��ˮ��ͨ�����������̼��Ca2����2OH����CO2===CaCO3����H2O
D. ����������Һ��ϡ���ᷴӦ��Ba2����SO42-��H����OH��===BaSO4����H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���X��һ����Ҫ���л�����ԭ�ϣ���ͼ��ʾ�����л���XΪԭ����Ƶĺϳ�·��(���ֲ������ϳ�·�ߡ���Ӧ��������ȥ)��

��֪����.XΪ������������Է�������Ϊ92��Y��һ�ֹ��ܸ߷��Ӳ��ϡ�
��.����������Ը�����ص������£��������������Ȼ���![]() ��
��
��. ![]() (�������ױ�����)��
(�������ױ�����)��
����ݱ���������Ϣ����ѧ֪ʶ�ش��������⣺
(1)X�ṹ��ʽΪ________________��![]() �й����ŵ�����Ϊ______________��
�й����ŵ�����Ϊ______________��
(2)��Ӧ�۵ķ�Ӧ������__________����Ӧ�ں͢۵�˳���ܽ�����ԭ����_____________��
(3)��֪AΪһ�ȴ��
��Ӧ�ܵĻ�ѧ����ʽΪ___________________________��
��Ӧ�ݵ����ӷ���ʽΪ_________________________��
(4)��˾ƥ���ж���ͬ���칹�壬��������������ͬ���칹����___________ �֡�
�ٷ����廯����
�ڲ��ܷ���ˮ�ⷴӦ��Ҳ���ܷ���������Ӧ��
��1mol���л����������2molNaHCO3��ȫ��Ӧ��
(5)д����AΪԭ���Ʊ�![]() �ĺϳ�·������ͼ(�����Լ���ѡ)__________���ϳ�·������ͼ��ʾ�����£�
�ĺϳ�·������ͼ(�����Լ���ѡ)__________���ϳ�·������ͼ��ʾ�����£�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ�þ����Ҫ�������ϣ��ڳ���������ʪ��������ˮ���Ҵ���ij��ȤС���Ժ�ˮΪԭ���Ʊ���ˮ�Ȼ�þ��
ʵ��һ �Ʊ�MgCl2��6H2O����
�Ժ�ˮΪԭ�ϣ��������һϵ�д������õ����塣
��1����ȥ��ˮ�в��������ʳ��õ�ʵ�������______�������ƣ���
��2�����Ȼ�þ��Һ������MgCl2��6H2O����Ľᾧ������__________������½ᾧ���������ᾧ������
ʵ��� ��Ʒ��MgCl2��6H2O���庬���ⶨ
ȷ��ȡʵ��һ�Ƶõ�MgCl2��6H2O����a g����ƿ�У���ȥ����ˮ�ܽ⣬���μ���һ�������Ҵ�����NH3��NH4Cl������Һ��ҡ�ȣ��������Tָʾ������0.02000 mol��L��1EDTA����H2Y2����ʾ������Һ�ζ����յ㣬����EDTA��Һ�����VmL��
��֪����0.02000 mol��L��1EDTA����ҺpHԼΪ5��ָʾ������Tʹ�õ�����pH��ΧΪ8��11��NH3��NH4Cl������ҺpHԼΪ10��
�ڵζ�ԭ����Mg2++ H2Y2���� MgY2��+2H+��
��3��ʹ�õĵζ�����____________________���� ���ס����ҡ�����
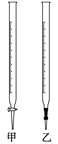
��4��NH3��NH4Cl������Һ��������_______________��
��5����Ʒ��MgCl2��6H2O����������Ϊ______________��
ʵ���� �Ʊ���ˮ�Ȼ�þ
������ͼʵ��װ�ã��гֺͼ���װ��ʡ�ԣ���ȷ��ȡһ������ MgCl2��6H2O������HCl������С�ļ��ȡ�
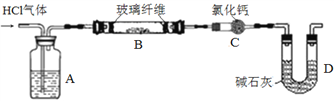
��6��Aװ�õ�������______________��
��7��ijͬѧ��ʵ��ǰ���ò�����B����m1g�������C����m2g��m1��m2������ܵ�ԭ����______________���û�ѧ����ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1L 0.1mol��L-1NaOH��Һ����0.07molCO2��������Һ��n(Na2CO3)��n(NaHCO3)֮��ԼΪ
A. 3�U4 B. 3�U1 C. 2�U3 D. 3�U2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����Na2SO3�����ֽ⣬ʵ�����̺ͽ�����£�
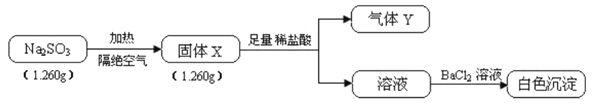
����Y��һ�ִ�����ڱ�״���µ��ܶ�Ϊ1.518g��L-1����ش�:
��1������Y���ӵĵ���ʽ___,��ɫ�����Ļ�ѧʽ_______��
��2���������е�Na2SO3���ȷֽ�Ļ�ѧ����ʽ__________��
��3����ȡ����X������Na2SO3��ϣ���ˮ�ܽ����ϡ���ᷴӦ���е���ɫ����������д����������ɫ���������ӷ���ʽ____________(�����ǿ�����Ӱ��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС������ͼ��ʾװ�òⶨ��þ�Ͻ������������������������ԭ��������
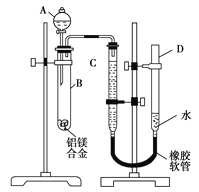
��1��A���Լ�Ϊ________��
��2��ʵ��ǰ���Ƚ���þ�Ͻ���ϡ���н���Ƭ������Ŀ����____________________��
��3���������������ҩƷ��ˮװ��������������Ӻ�װ�ú�������еIJ������У��ټ�¼C��Һ��λ�ã��ڽ�B��ʣ����������ϴ�������������أ��۴�B�в���������������ָ������º�����¼C��Һ��λ�ã�����A��B�еμ������Լ�������������˳����________(�����)����¼C��Һ��λ��ʱ����ƽ��������Ӧ________��
��4��B�з�����Ӧ�Ļ�ѧ����ʽΪ__________________________��
��5����ʵ������þ�Ͻ������Ϊa g������������Ϊb mL(�ѻ���Ϊ��״��)��B��ʣ����������Ϊc g�����������ԭ������Ϊ________��
��6��ʵ�����������δϴ�ӹ������õIJ�������������������������________(����ƫ������ƫС����������Ӱ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ھ��г��ͺĵ��������������ص㣬LED��ƷԽ��Խ���˻�ӭ����ͼ������ȼ�ϵ������LED�����װ�á������й�������ȷ����(����)

A. a��ͨ��������b��ͨ������
B. P�Ͱ뵼�����ӵ��ǵ�ظ���
C. ��������缫��ӦʽΪO2��2H2O��4e��===4OH��
D. ��װ����ֻ�漰������ʽ������ת��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com