
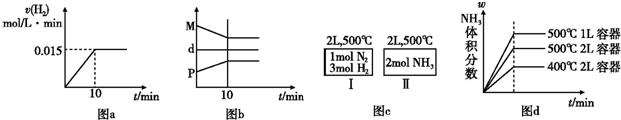
| A�����ﵽƽ��ʱ�������ϵ�ų�9.24 kJ��������H2��Ӧ���ʱ仯������ͼa��ʾ | B����Ӧ�����У��������ƽ����Է�������ΪM����������ܶ�Ϊd���������ѹǿΪP�����߹�ϵ��ͼb | C����ͼc��ʾ��������͢�ﵽƽ��ʱ��NH3���������Ϊ�أ���������ų���������������������֮��Ϊ92.4 kJ | D������ʼ��������Ϊ1 mol N2��3 mol H2���ڲ�ͬ�����´ﵽƽ��ʱ��NH3����������仯��ͼd��ʾ |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 2NH3�ǹ�ҵ�Ϻϳɰ�����Ҫ��Ӧ��
2NH3�ǹ�ҵ�Ϻϳɰ�����Ҫ��Ӧ��
 2NH3��g����H=2��E1-E3����-2��E3-E1��kg/mol
2NH3��g����H=2��E1-E3����-2��E3-E1��kg/mol 2NH3��g����H=2��E1-E3����-2��E3-E1��kg/mol
2NH3��g����H=2��E1-E3����-2��E3-E1��kg/mol| 16 |
| a2 |
| 16 |
| a2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 2 |
| 2-a |
| 2 |
| 2-a |
 2NH3��g��+92.2kJ/mol
2NH3��g��+92.2kJ/mol�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| 16 |
| a2 |
| 16 |
| a2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
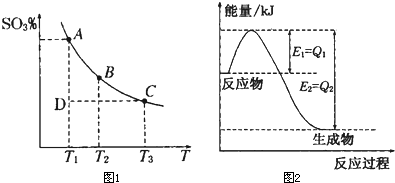
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
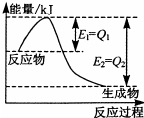 ���û�ѧ��Ӧԭ���о��������ȵȵ��ʼ��仯����ķ�Ӧ����Ҫ�����壮
���û�ѧ��Ӧԭ���о��������ȵȵ��ʼ��仯����ķ�Ӧ����Ҫ�����壮�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com