
 nZ(g) +2W(g)
nZ(g) +2W(g)科目:高中化学 来源: 题型:
 nZ(g)+2W(g)2min末,生成0.4mol W,以Z的浓度表示的反应速率为0.1mol/(L?min)
nZ(g)+2W(g)2min末,生成0.4mol W,以Z的浓度表示的反应速率为0.1mol/(L?min)查看答案和解析>>
科目:高中化学 来源:2012届浙江省东阳中学高三下学期阶段检测化学试卷 题型:填空题
“氢能”将是未来最理想的新能源。
Ⅰ.实验测得,1g氢气燃烧生成液态水时放出142.9kJ热量,则氢气燃烧的热化学方程式为_______。(填序号)
A.2H2(g)+O2(g)  2H2O(l)△H= -142.9kJ·mol—1 2H2O(l)△H= -142.9kJ·mol—1 |
B.H2(g)+1/2 O2(g)  H2O(l)△H= -285.8kJ·mol—1 H2O(l)△H= -285.8kJ·mol—1 |
C.2H2+O2 2H2O(l)△H= -571.6kJ·mol—1 2H2O(l)△H= -571.6kJ·mol—1 |
D.H2(g)+1/2 O2(g)  H2O(g) △H= -285.8kJ·mol—1 H2O(g) △H= -285.8kJ·mol—1 |
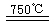 CaO+2HBr ②2HBr+Hg
CaO+2HBr ②2HBr+Hg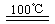 HgBr2+H2
HgBr2+H2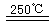 ______________ ④2HgO
______________ ④2HgO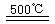 2Hg+O2↑
2Hg+O2↑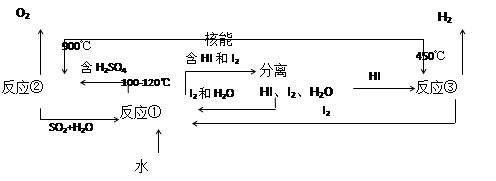
 CO2(g)+ H2(g); △H<0。
CO2(g)+ H2(g); △H<0。查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:2009-2010学年吉林省长春外国语学校高一(下)期末化学试卷(理)(解析版) 题型:解答题
 nZ(g)+2W(g)2min末,生成0.4mol W,以Z的浓度表示的反应速率为0.1mol/
nZ(g)+2W(g)2min末,生成0.4mol W,以Z的浓度表示的反应速率为0.1mol/查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com