
 如图所示,A为直流电源,B为渗透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:
如图所示,A为直流电源,B为渗透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:分析 (1)由B上的c点显红色判断c的电极,根据c的电极判断a、b的电极;
(2)根据溶液中离子的放电顺序判断生成物,由反应物、生成物写出相应的方程式;
(3)先判断e、f的电极,再根据阴阳极上发生的反应写出相应的电极反应式.
解答 解:(1)B外接电源,所以是电解氯化钠溶液的电解池,接通电路后,发现B上的c点显红色,B上的c点显红色,说明c点有氢氧根离子生成,根据离子的放电顺序知,该极上氢离子得电子放电,所以c是阴极,外电源b是负极,a是正极,
故答案为:正;
(2)电解氯化钠溶液时,溶液中的离子放电顺序为:氢离子放电能力大于钠离子,氯离子放电能力大于氢氧根离子,所以电解氯化钠时生成物是氯气、氢气、氢氧化钠,所以其反应方程式为 2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑,
故答案为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑;
(3)电镀时,e是阳极,f是阴极,镀层锌作阳极,镀件铁作阴极,阳极上失电子变成离子进入溶液,阴极上锌离子得电子生成锌单质,所以阳极上电极反应式为Zn-2e-=Zn2+;故答案为:锌;Zn-2e-═Zn2+.
点评 本题考查了电解原理与电镀池,判断电极是关键,离子掌握溶液中离子的放电顺序及电极反应方程式书写,难度中等.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 将1mol铁粉加入到一定量的稀硝酸溶液中充分反应,转移的电子数一定是3NA | |
| B. | 标准状况下,22.4L己烷中共价键数目为19NA | |
| C. | 由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA | |
| D. | 1.0 L 1.0 mol•L-1 NaClO溶液中含有ClO-离子的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 品红的分子式为C20H19N3 | |
| B. | 上述漂白原理反应属加成反应 | |
| C. | 碱性品红及其与H2SO3生成的无色化合物都可与NaOH溶液反应 | |
| D. | 碱性品红与H2SO3生成的无色化合物不稳定,加热后恢复原来的颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 反应完成后,O2有剩余 | |
| B. | 原混合气体中,C2H4与C2H2的体积共为1.9L | |
| C. | 反应完成后,生成水的质量为9g | |
| D. | 原混合气体中,CO与CH4的体积比一定为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
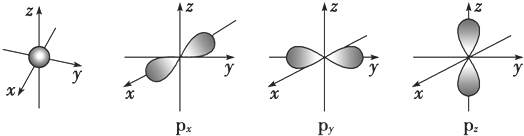
 .若元素X的原子最外层电子排布式为nsn-1npn+1,那么X的元素符号为S,原子的电子排布图为
.若元素X的原子最外层电子排布式为nsn-1npn+1,那么X的元素符号为S,原子的电子排布图为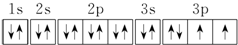 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1NaCl溶液中含有0.1nA个Na+ | |
| B. | 标准状况下,22.4 L 苯含有nA个苯分子 | |
| C. | 7.8 g Na2O2与足量水反应转移0.2nA个电子 | |
| D. | 标准状况下,2.24 LCH4和C2H4混合气体中含有的H原子数为0.4nA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | Y | Z | |
| I1 | 496 | 738 | 577 |
| I2 | 4562 | 1451 | 1817 |
| I3 | 6912 | 7733 | 2754 |
| 9540 | 10540 | 11578 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com