
| A.浓硫酸 | B.浓盐酸 | C.稀硫酸 | D.稀盐酸 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.S的漂白性 | B.S的还原性 |
| C.SO2的漂白性 | D.SO2的还原性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.24.5g/L | B.14.4g/L | C.8g/L | D.5.1g/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
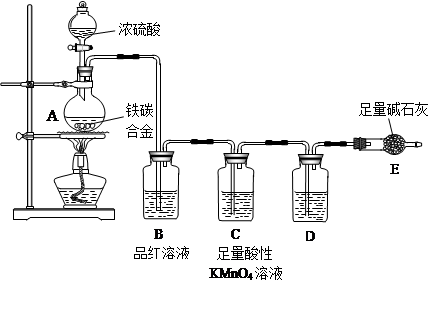
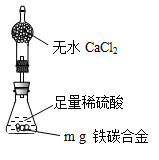
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.④⑤ | B.②④ | C.② | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
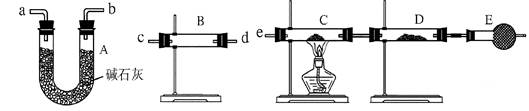
| 装置 | 所盛药品 | 实验现象 | 结论或解释 |
| B | | | |
| C | CuO固体 | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
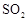 转化为
转化为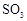 的转化率测定实验:
的转化率测定实验: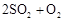
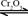
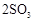 ;
;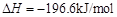 。已知:
。已知:| | 熔点(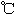 ) ) | 沸点(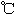 ) ) |
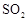 | -72.4 | -10 |
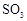 | 16.8 | 44.3 |
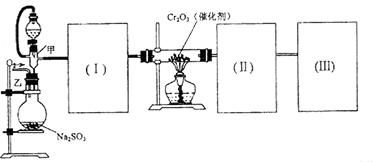
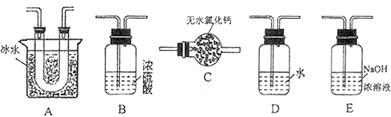
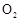 ,为使
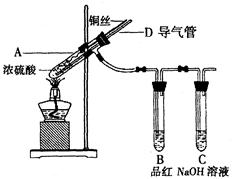
,为使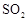 有较高的转化率,实验时滴入浓硫酸与加热催化剂的先后顺序是 。
有较高的转化率,实验时滴入浓硫酸与加热催化剂的先后顺序是 。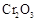 表面红热时,应将酒精灯移开一会儿再加热”,以防温度过高,这样做的原因是 ;若用大火加热有
表面红热时,应将酒精灯移开一会儿再加热”,以防温度过高,这样做的原因是 ;若用大火加热有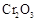 处的反应管时,
处的反应管时,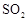 的转化率会 (填“升高”、“降低”或“不变”)。
的转化率会 (填“升高”、“降低”或“不变”)。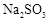 ,加入的浓硫酸是足量的,反应结束时继续通入
,加入的浓硫酸是足量的,反应结束时继续通入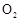 一段时间,称得Ⅱ处装置的质量增加11.3g,则本实验中
一段时间,称得Ⅱ处装置的质量增加11.3g,则本实验中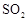 的转化率为 %(保留小数点后一位)。
的转化率为 %(保留小数点后一位)。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
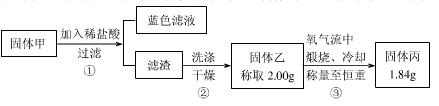
| A.固体甲中,CuS和Cu2S不能同时存在 |
| B.固体甲中,CuO和Cu2O至少有一种 |
| C.固体甲中若没有Cu2O,则一定有Cu2S |
| D.固体甲中可能有Cu2S |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.可以用澄清石灰水鉴别SO2和CO2 |
| B.硫粉在过量的纯氧中燃烧可以生成SO3 |
| C.SO2能使溴水、酸性KMnO4溶液退色 |
| D.少量SO2通过浓的CaCl2溶液能生成白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com