
 CH3OH↙g⇄@H
CH3OH↙g⇄@H| 梁業 | 250°C | 300°C | 350°C |
| K | 2.041 | 0.270 | 0.012 |
| 否匂 | 遮 | 厰 | 央 | |
| 郡哘麗誘秘楚 | 1molCO、2moL H2 | 1molCH3OH | 2molCH3OH | |
| 峠 財 扮 議 方 象 | CH3OH敵業↙mol/L⇄ | c1 | c2 | c3 |
| 郡哘議嬬楚延晒 | akJ | bkJ | ckJ | |
| 悶狼儿膿↙Pa⇄ | p1 | p2 | p3 | |
| 郡哘麗廬晒楕 | α1 | α2 | α3 | |
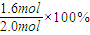 =80%⇧夸
=80%⇧夸 CH3OH↙g⇄
CH3OH↙g⇄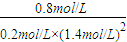 =2.041↙mol/L⇄-2⇧梁業哘葎250≧⇧
=2.041↙mol/L⇄-2⇧梁業哘葎250≧⇧ CH3OH↙g⇄
CH3OH↙g⇄ mol/L
mol/L 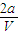 mol/L O
mol/L O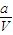 mol/L
mol/L 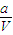 mol/L 0.5×
mol/L 0.5×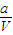 mol/L
mol/L 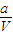 mol/L
mol/L 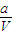 mol/L 0.5×
mol/L 0.5×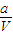 mol/L
mol/L 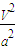 ⇧
⇧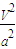 ◉﨑剃郡哘圭﨑◉受弌◉
◉﨑剃郡哘圭﨑◉受弌◉

 剩高仁銘仁扮恬匍狼双基宛
剩高仁銘仁扮恬匍狼双基宛親朕⦿互嶄晒僥 栖坿⦿ 籾侏⦿堋響尖盾
 CH3OH↙g⇄@H
CH3OH↙g⇄@H| 梁業 | 250<C | 300<C | 350<C |
| K | 2.041 | 0.270 | 0.012 |
| V2 |
| a2 |
| V2 |
| a2 |
| 否匂 | 遮 | 厰 | 央 | |
| 郡哘麗誘秘楚 | 1molCO、2moL H2 | 1molCH3OH | 2molCH3OH | |
| 峠 財 扮 議 方 象 |
CH3OH敵業↙mol/L⇄ | c1 | c2 | c3 |
| 郡哘議嬬楚延晒 | akJ | bkJ | ckJ | |
| 悶狼儿膿↙Pa⇄ | p1 | p2 | p3 | |
| 郡哘麗廬晒楕 | α1 | α2 | α3 | |
臥心基宛才盾裂>>
親朕⦿互嶄晒僥 栖坿⦿采臼福財邦嶄僥2010⇩2011僥定互匯和僥豚豚挑深編晒僥編籾 籾侏⦿022
| |||||||||||||||||||||||||||||||
臥心基宛才盾裂>>
親朕⦿互嶄晒僥 栖坿⦿音峋 籾侏⦿諒基籾

| 梁業 | 250<C | 300<C | 350<C |
| K | 2.041 | 0.270 | 0.012 |
| 否匂 | 遮 | 厰 | 央 | |
| 郡哘麗誘秘楚 | 1molCO、2moL H2 | 1molCH3OH | 2molCH3OH | |
| 峠 財 扮 議 方 象 |
CH3OH敵業↙mol/L⇄ | c1 | c2 | c3 |
| 郡哘議嬬楚延晒 | akJ | bkJ | ckJ | |
| 悶狼儿膿↙Pa⇄ | p1 | p2 | p3 | |
| 郡哘麗廬晒楕 | α1 | α2 | α3 | |
臥心基宛才盾裂>>
刷臼福札選利離隈才音措佚連訟烏峠岬 | 利貧嗤墾佚連訟烏廨曝 | 窮佚姨騰訟烏廨曝 | 膚煽雰倡涙麼吶嗤墾佚連訟烏廨曝 | 膚二盃幡訟烏廨曝
離隈才音措佚連訟烏窮三⦿027-86699610 訟烏喨屺⦿58377363@163.com