
���� ��A��B��C��D��E����������Һ����������ˮ��ԭ����֪��ǿ��������ˮ������ԣ�ǿ��������ˮ��ʼ��ԣ�NH4+��Al3+��Ag+Ϊ���������ӣ�K+��Ba2+Ϊǿ�������ӣ�Cl-��Br-��NO3-��SO42-Ϊǿ������ӣ�CO32-Ϊ��������ӣ�����Ag+ֻ��NO3-��ϳ�AgNO3��Һ��Ba2+����SO42-��CO32-���ϣ�AgBrΪdz��ɫ������B����Һ��c��OH-����c��H+����B��Һ�ʼ��ԣ�ֻ����ǿ����������Һ�����Ƶ�ΪK2CO3���ܹ�����˫ˮ�ⷴӦ������Ϊ��2Al3++3CO32-+3H2O�T2Al��OH��3��+CO2����������Ŀ��֪����������⣮
��� �⣺��1����������C��D��E������Һ��pH��7��˵��C��D��E������ҺΪǿ�������Σ�ˮ������ԣ�B��Һ�ʼ��ԣ�A����Һ�����ԣ�Ag+����Cl-��Br-��SO42-��CO32-���ϣ���ΪAgCl��Ag2SO4��Ag2CO3��Ϊ��ɫ������AgBrΪdz��ɫ������ֻ���γ������������Ʋ�֪AΪ������Һֻ���Ȼ���������B����Һ��c��OH-����c��H+����Һ�ʼ��ԣ�BΪǿ�������Σ���K+��Ba2+Ϊǿ�������ӣ�CO32-Ϊ��������ӣ����Bֻ��ΪK2CO3������B��C��Ӧ���ɰ�ɫ���������壬B�к�CO32-��������CO32-��Ӧ���ɳ�������Al3+��Ag+��Ba2+������CO32-��Al3+����˫ˮ�ⷴӦ�������ɳ��������������壬���ӷ�ӦΪ2Al3++3CO32-+3H2O�T2Al��OH��3��+CO2��������C�к�Al3+����CΪǿ��������������Һ���������ΪCl-��Br-��SO42-�е�һ�֣���Ϊ������������A�ɷֱ���B��D��Ӧ���ɰ�ɫ������BΪK2CO3��CΪ��������D��ֻ������������EΪNH4Br��
�ʴ�Ϊ��Al2��SO4��3��AgNO3��NH4Br��
��2��BΪK2CO3����Һ��CO32-����ˮ�ⷴӦ����CO32-+H2O?HCO3-+OH-��ʹ��Һ�ʼ��ԣ�����c��OH-����c��H+����
����Һ��CO32-����ˮ�ⷴӦ����CO32-H2O?HCO+OH-��ʹ��Һ�ʼ��ԣ�����c��OH-����c��H+����
���� ���⿼������ˮ�⡢˫ˮ�⡢���ӷ���ʽ�����ӷ�Ӧ�����ݣ������Ŀ�е���Ϣ����Һ�ʼ��ԡ����ɰ�ɫ������������ǽ���ؼ���ͬʱǰ����ϵ�����ھ������������Ϣ�����ܼ������������⣬��Ŀ�Ѷ��еȣ�


 �������Ͽ��㱾ϵ�д�
�������Ͽ��㱾ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | Cu��OH��2 | Fe��OH��3 | CuCl | CuI |
| Ksp | 2.2��10-20 | 2.6��10-39 | 1.7��10-7 | 1.3��10-12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | �� | �� | �� | |||||
| 3 | �� | �� | �� | �� | �� | |||
| 4 | �� | �� |
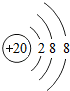 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
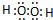 ���÷��Ӻ��м��Լ��ͷǼ��Լ�������ԡ������Ǽ��ԡ�����
���÷��Ӻ��м��Լ��ͷǼ��Լ�������ԡ������Ǽ��ԡ������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 CaCl2
CaCl2 N2
N2 OH-
OH-
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | a-c=m-n | B�� | a-b=n-m | C�� | c+d=m+n | D�� | b-d=n+m |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
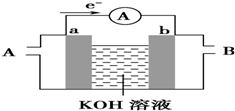 ��1�����������һ�����Ϳɳ���أ�����ͨ�����ȣ��õ���ܽϳ�ʱ�䱣���ȶ��ķŵ��ѹ��������ص��ܷ�ӦΪ��3Zn+2K2FeO4+8H2O $?_{���}^{�ŵ�}$3Zn��OH��2+2Fe��OH��3+4KOH�� ��ش��������⣺
��1�����������һ�����Ϳɳ���أ�����ͨ�����ȣ��õ���ܽϳ�ʱ�䱣���ȶ��ķŵ��ѹ��������ص��ܷ�ӦΪ��3Zn+2K2FeO4+8H2O $?_{���}^{�ŵ�}$3Zn��OH��2+2Fe��OH��3+4KOH�� ��ش��������⣺�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com