
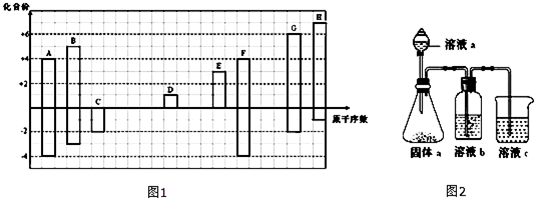
分析 短周期元素中,A、F均有+4、-4价,处于ⅣA族,且原子序数A<F,故A为碳、F为Si;C、G均有-2价,且G有+6,G的原子序数较大,故C为O元素、G为S元素;B有+5、-3价,原子序数介于碳、氧之间,故B为N元素;H有+7、-1价,原子序数大于硫,则H为Cl;D有+1价,E有+3价,分别处于ⅠA族、ⅢA族,原子序数氧<D<E<Si,故D为Na,E为Al,由此分析解答.
解答 解:短周期元素中,A、F均有+4、-4价,处于ⅣA族,且原子序数A<F,故A为碳、F为Si;C、G均有-2价,且G有+6,G的原子序数较大,故C为O元素、G为S元素;B有+5、-3价,原子序数介于碳、氧之间,故B为N元素;H有+7、-1价,原子序数大于硫,则H为Cl;D有+1价,E有+3价,分别处于ⅠA族、ⅢA族,原子序数氧<D<E<Si,故D为Na,E为Al.
(1)元素F为Si,在周期表中的位置:第三周期ⅣA族,故答案为:第三周期ⅣA族;
(2)O与Na形成原子个数比为1:1的化合物是过氧化钠,过氧化钠中所含有离子键、非极性共价键,故答案为:离子键、非极性共价键;
(3)电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越小,简单离子半径大小顺序是:S2->O2->Na+,故答案为:S2->O2->Na+;(4)利用最高价含氧酸的酸性强弱,证明A、B、F的非金属性强弱关系,溶液a为硝酸,溶液b为饱和NaHCO3溶液,溶液c为硅酸钠溶液,溶液c中的离子反应方程式为:SiO32-+CO2+H2O=H2SiO3↓+CO32-或SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-,
故答案为:①硝酸;饱和NaHCO3溶液;②SiO32-+CO2+H2O=H2SiO3↓+CO32-或SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-.
点评 本题考查结构性质位置关系应用,关键是根据化合价与原子序数推断元素,注意对元素周期律的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | 常温下,pH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序为c(Cl-)>c(NH+4)>c(H+)>c(OH-) | |
| B. | 将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 | |
| C. | 常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 | |
| D. | 将pH=4的醋酸溶液和pH=10的氢氧化钠溶液等体积混合,所得溶液的pH一定大于7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. (或
(或 )(写出任一种的结构简式).
)(写出任一种的结构简式). .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
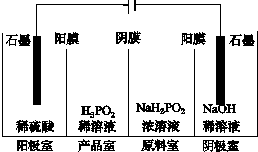 次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性.回答下列问题:
次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把绿豆大的钾投入水中 | |
| B. | 把除去氧化膜的镁带放入少量冷水中 | |
| C. | 把溴水滴加到KI溶液中,并加入少量四氯化碳溶液 | |
| D. | 把铜片和铁片紧靠在一起浸入稀硫酸中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂的水解 | |
| B. | 在一定条件下,苯与浓硝酸反应制取硝基苯 | |
| C. | 乙醛与氢气的反应 | |
| D. | 甲烷与氯气在光照条件下反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①②④⑤ | C. | ②⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
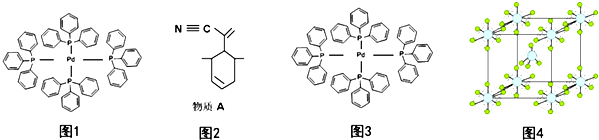
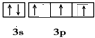 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 侯德榜--创立了联合制碱法 | |
| B. | 凯库勒--首次提出了“有机化学”概念 | |
| C. | C维勒--首次用无机物合成了有机物 | |
| D. | 门捷列夫--创设了元素周期表 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com