
(思维拓展题)CH2Br-CH2Br可作汽油抗爆剂的添加剂,常温下是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.试管b中装有液溴(表面覆盖少量水).工业用乙烯中常含少量H2S气体.利用工业乙烯通过下列装置可制备少量CH2Br-CH2Br.
填写下列空白.
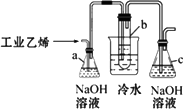
(1)容器a中NaOH溶液的作用是________.
(2)写出本题中制备CH2Br-CH2Br的化学方程式________,该反应属于________反应(填反应类型).
(3)解释将试管b放入盛有冷水的烧杯中的理由:________.
(4)某学生在做此实验时,使用一定量的液溴.当溴全部褪色时,所消耗工业乙烯的量比正常情况下超出许多.试分析其可能的原因________.
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解
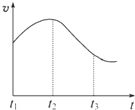 (思维拓展题)某研究学习小组为探究锌与盐酸反应,取同质量、同体积的锌片、同浓度盐酸做了下列平行实验:
(思维拓展题)某研究学习小组为探究锌与盐酸反应,取同质量、同体积的锌片、同浓度盐酸做了下列平行实验:| 负极材料 | 正极材料 | 负极反应式 | 正极反应式 | 电解质溶液 | |
| 实验三 | Zn | 杂质 | Zn-2e-=Zn2+ | 2H++2e-=H2↑ | 盐酸 |
| 实验四 | Zn | Cu | Zn-2e-=Zn2+ | 2H++2e-=H2↑ | 盐酸 |
| 负极材料 | 正极材料 | 负极反应式 | 正极反应式 | 电解质溶液 | |
| 实验三 | Zn | 杂质 | Zn-2e-=Zn2+ | 2H++2e-=H2↑ | 盐酸 |
| 实验四 | Zn | Cu | Zn-2e-=Zn2+ | 2H++2e-=H2↑ | 盐酸 |
查看答案和解析>>
科目:高中化学 来源:高一化学 专题1 微观结构与物质的多样性 1.1.3元素周期表及其应用(苏教版必修2) 题型:013
|
(思维拓展题)甲、乙是周期表中同一主族的两种元素,若甲的原子序数为x,则乙的原子序数不可能是 | |
| [ ] | |
A. |
x+2 |
B. |
x+4 |
C. |
x+8 |
D. |
x+18 |
查看答案和解析>>
科目:高中化学 来源:高一化学 专题1 微观结构与物质的多样性 1.1.1原子核外电子的排布(苏教版必修2) 题型:022
(思维拓展题)甲、乙、丙、丁是1~18号元素,乙元素原子有3个电子层,第一层与最外层电子数相等;甲元素原子的核外电子数比乙元素原子的核外电子数少1;丙元素原子的最外层电子数是次外层电子数的2倍;丁元素原子核电荷数比丙元素原子核电荷数多2.请回答:
(1)甲的单质与水反应的化学方程式为________;
(2)乙元素的原子结构示意图为________;
(3)丙元素的最高价氧化物可以和甲与丁两种元素形成的某种化合物反应生成丁单质,每生成1 mol丁单质,转移电子的数目约为________.
(4)写出一个能够证明乙单质的还原性比丙单质的还原性强的化学方程式________.
查看答案和解析>>
科目:高中化学 来源:《第2章 化学反应与能量》2011年单元测试卷(南阳一中)(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com