
已知Ksp(BaSO4 )= 1.1×10-10,Ksp(BaCO3)=2.5×10-9。下列说法中不正确的是
| A.BaSO4比BaCO3溶解度小,所以,BaCO3可以转化为BaSO4 |
| B.BaCO3、BaSO4均不溶于水,所以都可以做钡餐试剂 |
| C.向Na2CO3溶液中加入BaCl2和Na2SO4,当两种沉淀共存时,c(SO42—)/ c(CO32—) =4.4×10-2 |
| D.常温下,BaCO3若要在Na2SO4溶液中开始转化为BaSO4,则Na2SO4的浓度必须不低于2.2×10-6 mol·L-1 |
B
解析试题分析:根据硫酸钡和碳酸钡的组成以及硫酸钡的溶度积常数小于碳酸钡的溶度积常数可知,BaSO4比BaCO3溶解度小,所以,BaCO3可以转化为BaSO4,A正确;碳酸钡能溶于酸中,不能用作钡餐,选项B不正确;向Na2CO3溶液中加入BaCl2和Na2SO4,当两种沉淀共存时,溶液中Ba2+浓度相等,则Ksp(BaSO4 )÷Ksp(BaCO3)=c(SO42—)/ c(CO32—)=1.1×10-10÷2.5×10-9=4.4×10-2,C正确;根据溶度积常数可知,在碳酸钡溶液中,Ba2+浓度=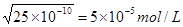 ,所以常温下,BaCO3若要在Na2SO4溶液中开始转化为BaSO4,则Na2SO4的浓度必须不低于
,所以常温下,BaCO3若要在Na2SO4溶液中开始转化为BaSO4,则Na2SO4的浓度必须不低于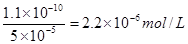 ,D正确,答案选B。
,D正确,答案选B。
考点:考查难溶电解质的溶解平衡和沉淀转化
点评:该题是高考中的常见图像,属于中等难度的试题。试题综合性强,主要是考查学生对溶解平衡以及溶度积常数计算、沉淀转化的沉淀,旨在培养学生分析、归纳和总结问题的能力,有利于培养学生的逻辑推理能力和创新思维能力。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高二上学期期末考试化学试卷(解析版) 题型:选择题
某温度下,已知Ksp(BaSO4 )= 1.1×10-10,Ksp(BaCO3)=2.5×10-9。下列说法正确的是
A.BaSO4比BaCO3溶解度小,所以,BaCO3 不可能转化为BaSO4
B.BaCO3 、BaSO4均不溶于水,所以都可以做钡餐试剂
C.任何温度下,向Na2CO3溶液中加入BaCl2和Na2SO4,当两种沉淀共存时,c(SO42—)/ c(CO32—) =4.4×10-2
D.该温度下,BaCO3若要在Na2SO4溶液中转化为BaSO4,则Na2SO4浓度至少为2.2×10-6 mol·L
查看答案和解析>>
科目:高中化学 来源:2014届江苏省扬州市高二下学期期末考试化学试卷(解析版) 题型:选择题
已知Ksp(BaSO4 )= 1.1×10-10,Ksp(BaCO3)=2.5×10-9。下列说法中不正确的是
A.BaSO4比BaCO3溶解度小,所以,BaCO3可以转化为BaSO4
B.BaCO3、BaSO4均不溶于水,所以都可以做钡餐试剂
C.向Na2CO3溶液中加入BaCl2和Na2SO4,当两种沉淀共存时,c(SO42—)/ c(CO32—) =4.4×10-2
D.常温下,BaCO3若要在Na2SO4溶液中开始转化为BaSO4,则Na2SO4的浓度必须不低于2.2×10-6 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省济宁市高三上学期期末模拟化学试卷(解析版) 题型:填空题
(10分)运用相关原理,回答下列各小题:
(1)25℃时,某FeCl3溶液的pH=2,则由水电离产生的总c(OH-)= ;用离子方程式表示FeCl3溶液用于净水的原因 。
(2)已知NaHSO4在水中的电离方程式NaHSO4=Na++H++SO42-。
在NaHSO4溶液中c(H+) c(OH-)+c(SO42-)(填“>”、“=”或“<”下同);用硫酸氢钠与氢氧化钡溶液制取硫酸钡,若溶液中SO42-完全沉淀,则反应后溶液的pH 7。
(3)将0.02mol/LNa2SO4溶液与某浓度BaCl2溶液等体积混合,则生成BaSO4沉淀所需原BaCl2溶液的最小浓度为 。(已知Ksp(BaSO4)=1.1×10-10)
(4)写出下列反应的化学方程式:
苯的硝化反应 。 乙醇的催化氧化反应 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com