
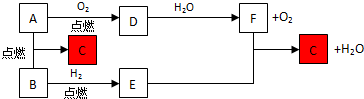
分析 A、B为常见物质,D为淡黄色固体,D与水反应生成F和氧气;可知D为过氧化钠,又因为C的水溶液与硝酸银溶液反应有白色沉淀生成,可知A为钠,B为氯气,C为氯化钠,E为氯化氢,F为氢氧化钠.
(1)钠为11号元素,质子数为11,有3个电子层;
(2)依据离子化合物、共价化合物概念判断;
(3)氯化氢与氢氧化钠反应生成氯化钠和水,结合反应特点及复分解反应定义判断.
解答 解:A、B为常见物质,D为淡黄色固体,D与水反应生成F和氧气;可知D为过氧化钠,又因为C的水溶液与硝酸银溶液反应有白色沉淀生成,可知A为钠,B为氯气,C为氯化钠,E为氯化氢,F为氢氧化钠.
(1)钠为11号元素,质子数为11,有3个电子层,所以其在周期表中位置:第三周期,ⅠA族;
故答案为:第三周期,ⅠA族;
(2)氯化钠是由钠离子与氯离子通过离子键结合而成的化合物,符合离子化合物概念,属于离子化合物;
故答案为:离子;
(3)氯化氢与氢氧化钠反应生成氯化钠和水,离子方程式:H++OH-=H2O,符合复分解反应定义,属于复分解反应;
故答案为:H++OH-=H2O;复分解反应.
点评 本题通过无机框图推断,考查了元素周期表结构、离子化合物、共价化合物判断、物质的性质等,题目难度不大,熟悉常见物质的性质及结构特点是解题关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 如图是钾、氧两元素形成的一种晶体的一个晶胞(晶体中最小的重复单元).晶体中氧的化合价可看作是部分为0价,部分为-2价.
如图是钾、氧两元素形成的一种晶体的一个晶胞(晶体中最小的重复单元).晶体中氧的化合价可看作是部分为0价,部分为-2价.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢键比范德华力强,所以它属于化学键 | |
| B. | 分子间形成的氢键使物质的熔点和沸点升高 | |
| C. | HF分子内存在氢键 | |
| D. | H2O是一种稳定的化合物,这是由于H2O之间形成氢键所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 项目 | 乙炔水化法 | 乙烯氧化法 |
| 原料 | 乙炔、水 | 乙烯、空气 |
| 反应条件 | HgSO4(催化剂) 100℃~125℃ | PdCl2~CuCl2(催化剂) 100℃~125℃ |
| 平衡转化率 | 乙炔转化率 90% | 乙烯转化率 80% |
| 反应速率 | 较 慢 | 较 快 |
| 原料来源生产工艺 | CaCO3$\stackrel{高温}{→}$CaO$\stackrel{+C电炉}{→}$ CaC2$\stackrel{饱和食盐水}{→}$C2H2 | 石油裂解气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
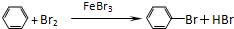
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com